过氧化氢酶(CAT)活性检测:紫外法与比色法(微量法)哪个更适合你的实验?
选方法,其实是在选"你测到的究竟是什么"
过氧化氢酶(CAT, EC 1.11.1.6)活性检测是氧化应激研究中的基础实验之一,无论是植物逆境生理、动物疾病模型还是细胞培养体系的抗氧化评价,几乎都绑定着这一指标。打开文献搜索引擎,你会发现不同实验室报告CAT活性时所用的方法并不统一——有的在240 nm处直接追踪H₂O₂的分解动力学,有的在540 nm处做终点比色。这两类方法在原理上有着根本性的差异,而这种差异直接决定了你测到的信号究竟在多大程度上反映真实的CAT活性。
这不是一个纯粹的学术讨论。如果你正在为课题组采购CAT活性检测试剂盒,或者在建立方法体系时犹豫应该走哪条技术路线,那么理解两种方法的底层逻辑、各自的适用边界和潜在干扰源,是做出正确选择的前提。
先搞清楚一件事:CAT有两种催化功能
要理解两种检测方法的差异,首先需要了解CAT本身的催化机制。CAT是一种含铁卟啉辅基的四聚体酶,它的活性中心可以执行两种截然不同的催化反应。
第一种是催化功能(catalatic activity),即经典的歧化反应:
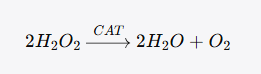
在这一反应中,第一个H₂O₂分子将CAT活性中心的Fe³⁺氧化为高价铁-氧中间体(Compound I),第二个H₂O₂分子随即将Compound I还原回基态,同时释放一分子O₂和一分子H₂O。这个反应的底物转换数(turnover number)极高,可达每秒数百万分子H₂O₂,是已知反应速率最快的酶促反应之一。
第二种是过氧化物酶功能(peroxidatic activity),反应方程式为:
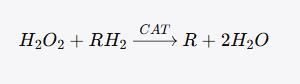
在这一反应中,H₂O₂仍然将CAT活性中心氧化为Compound I,但不是由第二个H₂O₂来完成还原,而是由一个小分子醇类(如甲醇、乙醇)作为氢供体,将Compound I还原回基态。当氢供体是甲醇时,反应产物为甲醛。
这两种功能在生理条件下的主导地位取决于H₂O₂浓度:在高H₂O₂浓度下(>100 µM),催化功能占主导;而在低H₂O₂浓度下,过氧化物酶功能变得更加活跃。两种检测方法正是分别针对这两种功能设计的。
紫外法:直接追踪H₂O₂分解的经典思路
原理
紫外法(也叫直接分光光度法、Aebi法)基于CAT的催化功能。H₂O₂在240 nm处有特征吸收,摩尔消光系数约为43.6 M⁻¹cm⁻¹。向反应体系中加入H₂O₂作为底物,加入含CAT的样本后,H₂O₂被分解,240 nm处的吸光度随时间线性下降。通过单位时间内吸光度的下降速率(ΔA240/min),结合消光系数和光程,即可计算出CAT活性。
这个方法由Hugo Aebi在1984年系统建立,至今仍是教科书上的"标准方法",在文献中的引用量极高。
优势
紫外法的核心优势在于操作简洁和成本低廉。反应体系极其简单——磷酸盐缓冲液加H₂O₂再加样本,就构成了完整的反应。不需要偶联试剂、显色底物或标准曲线,只要有一台能在240 nm处读数的紫外分光光度计即可完成检测。对于已经具备紫外分光光度计的实验室来说,这几乎是"零试剂成本"的方案。此外,由于直接检测底物消耗速率,紫外法在动力学分析上具有天然优势——如果你的研究目的是测定CAT的Km值、Vmax等酶动力学参数,紫外法提供的是连续实时动力学数据,比终点法更适合。
局限性
然而,紫外法有几个在生物样本检测中不可忽视的问题。
第一个问题是特异性不足。紫外法测量的是"H₂O₂消失的速率",但并非只有CAT能分解H₂O₂。生物体内至少存在三大类可以清除H₂O₂的酶体系:CAT、谷胱甘肽过氧化物酶(GPx)家族以及过氧化物还原酶(Prx)家族。在细胞裂解液或组织匀浆这种复杂基质中,GPx和Prx也会参与H₂O₂的清除。虽然紫外法通常使用较高浓度的H₂O₂(通常10-30 mM),这一浓度范围超出了GPx的最适底物浓度区间(GPx的Km约为1-10 µM H₂O₂),理论上可以最小化GPx的贡献,但并不能完全消除干扰——特别是在GPx表达水平很高的组织(如肝脏、肾脏)中。更重要的是,Prx 2在红细胞中含量极高且对H₂O₂有较高的催化效率。如果血液样本或灌流不充分的组织样本使用紫外法检测,Prx 2的贡献可能被错误计入CAT活性。
第二个问题是紫外区域的背景干扰。240 nm处于紫外区的深处,而生物样本中大量物质在这一波段有吸收:核酸在260 nm有吸收峰,蛋白质在280 nm有吸收峰,它们的吸收尾端都会延伸到240 nm附近。细胞裂解液中残留的DNA/RNA片段、游离核苷酸、以及高浓度的蛋白质,都会在240 nm处贡献背景吸光度。如果样本的背景OD240过高(>0.5),不仅会压缩可检测的动态范围,还可能导致检测器进入非线性区域。对于植物组织匀浆,情况更加棘手——酚类化合物、类黄酮等次生代谢产物在紫外区有强吸收,且这些物质本身可能具有非酶促的H₂O₂清除能力,进一步干扰结果。
第三个问题是对石英比色皿的依赖和低通量。240 nm的检测波长要求使用石英比色皿,普通玻璃或聚苯乙烯比色皿在这一波段会产生严重吸收。同时,传统紫外法通常在单光束或双光束分光光度计上逐个样本进行,每个样本需要记录至少1-3 min的动力学曲线。如果一个实验有6个处理组、每组8个重复,仅正式检测就需要处理48个样本,加上预热仪器和清洗比色皿的时间,一个人操作可能需要大半天。在这期间,早期处理的样本已经在室温下放置了数小时,酶活性可能发生变化。
比色法(微量法):从过氧化物酶功能出发的另一条路
原理
比色法(微量法)利用的是CAT的过氧化物酶功能。反应体系中同时提供H₂O₂和甲醇作为底物,CAT以H₂O₂为氧化剂催化甲醇脱氢生成甲醛。反应终止后,加入Purpald(4-氨基-3-肼基-5-巯基-1,2,4-三唑)与甲醛反应生成双环杂环化合物,经高碘酸钾氧化后形成紫色产物,在540 nm处比色定量。通过甲醛标准曲线将OD540转换为甲醛浓度,进而计算CAT活性。
这一方法路线最初由Wheeler、Johansson等人在1990年代建立并发表于Analytical Biochemistry等期刊,后经多家试剂盒厂商优化为标准化的商品化试剂盒。
核心优势:为什么过氧化物酶功能路线具有更高的特异性?
这是两种方法之间最关键的差异点,值得展开讨论。
如前所述,紫外法面临的最大挑战在于无法区分CAT与其他H₂O₂清除酶的贡献。比色法巧妙地规避了这个问题,关键在于它的检测读出端不是H₂O₂的消失,而是甲醛的生成——而甲醛只有在CAT催化甲醇氧化时才会产生。
要理解这一点,需要回到酶催化的底物特异性层面。GPx的催化机制是通过硒代半胱氨酸活性中心,以GSH作为专一的还原性底物来还原H₂O₂(或有机过氧化物),其反应方程式为:
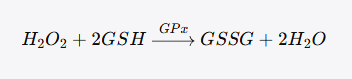
GPx对氢供体的选择极其严格——它只能利用GSH(或少数硫醇类化合物),完全不能利用甲醇作为氢供体。因此,在比色法的反应体系中,即使样本含有高活性的GPx,由于体系中不含GSH,GPx处于"无底物"状态,不会催化任何反应,更不会产生甲醛。
同样的逻辑适用于过氧化物还原酶(Prx)——Prx依赖硫氧还蛋白(Trx)系统提供还原力,在不含Trx和NADPH的反应体系中无法完成催化循环。其他过氧化物酶如髓过氧化物酶(MPO)、乳过氧化物酶(LPO)等虽然也有过氧化物酶活性,但它们的氢供体偏好芳香胺类或卤化物,对甲醇的催化效率极低。
换言之,比色法通过选择甲醇作为CAT过氧化物酶功能的特异性氢供体,在反应层面就构建了一道"分子滤网"——只有CAT能够有效利用甲醇并产生甲醛信号,其他H₂O₂代谢酶即使存在于样本中也无法产生可检测的信号。这种方法学上的特异性是从反应机理本身保证的,而不是依赖抑制剂或封闭剂来排除干扰,因此是一种更为根本和可靠的解决方案。
从实验者的角度来说,这意味着什么?意味着你在使用比色法时,不需要额外担心以下问题:样本灌流是否充分(红细胞中的Prx 2不会干扰);GPx高表达组织(如肝脏、肾脏)中GPx的交叉贡献;不同处理组之间GPx或Prx表达水平的差异是否会混淆CAT活性的组间比较。对于需要横向比较不同组织或不同处理条件下CAT活性的实验来说,这种特异性优势尤为重要。
其他实操层面的优势
除了特异性之外,比色法在日常使用中还有以下几个显著优势。
在检测波长方面,540 nm处于可见光区,远离蛋白质和核酸的吸收峰,因此几乎不受生物样本背景吸收的干扰。这一点在检测植物组织样本时格外重要——植物提取液中大量存在的酚类、黄酮类化合物在紫外区有强吸收,用紫外法检测时背景噪音极高,而在540 nm处这些物质几乎透明。同理,对于含有血红蛋白残留的动物组织样本,虽然血红蛋白在可见光区(405 nm Soret带)有一定吸收,但在540 nm处的干扰已经相当有限,远不及紫外区严重。
在通量方面,比色法天然适配96孔微孔板格式。一块板可以同时处理40-80个样本(含标准曲线和对照),所有孔在相同时间段内完成反应和读数,消除了紫外法逐一检测时不可避免的时间漂移问题。对于动物实验中常见的多组别、多时间点设计,或者高通量药物筛选场景,96孔板格式在效率上具有压倒性的优势。
在样本用量方面,由于微孔板每孔反应体积通常在200-250 µL之间,每个反应孔仅需20 µL样本。相比之下,紫外法在标准比色皿(1 cm光程)中进行时,反应体积通常为1-3 mL,对应的样本用量在50-200 µL之间。当样本量有限——例如小鼠脑区微量组织、细胞培养上清液或稀有植物组织——比色法对样本的节约效果非常显著,也为同一份样本平行检测多项指标留出了余量。
需要了解的局限性
公允地说,比色法也并非没有局限。
首先,它是终点法而非连续动力学法。Purpald显色反应需要在碱性条件下进行(加入KOH终止酶促反应后才能显色),因此你得到的是"固定时间内累计生成的甲醛量",而不是实时的反应速率曲线。如果你的研究目标是精确测定CAT的酶动力学参数(Km、Vmax、抑制常数Ki等),紫外法提供的连续动力学数据在理论上更直接。不过对于绝大多数以"比较不同组别之间CAT活性差异"为目的的应用——这也是90%以上研究者的实际需求——终点法提供的信息已经完全足够。
其次,比色法涉及多步加样和显色,操作步骤比紫外法多。每个反应孔需要依次加入样本、Assay Buffer、甲醇、H₂O₂,孵育后还需加入KOH、Purpald和高碘酸钾。虽然每一步操作本身并不复杂,但步骤多意味着对移液精度和时间控制的要求更高。好在使用多通道移液器可以大幅提高效率并减少孔间差异,这也是为什么我们建议在96孔板中使用多通道操作的原因。
第三,Purpald显色反应对甲醛有一定的检测下限,这意味着在CAT活性极低的样本(如某些低表达CAT的细胞系或严重损伤的组织)中,信号可能接近空白值。对于这类情况,可以通过增加样本量(减少稀释倍数)或延长反应时间来提高信号强度,但需要在预实验中优化。
不同实验场景下的方法选择建议
了解了两种方法的原理和各自特点后,方法选择可以从实际实验场景出发进行判断。
如果你在做动物模型(如CCl₄肝损伤、高脂饮食、糖尿病等)的氧化损伤评价,需要比较多个处理组之间的CAT活性差异,首选比色法。理由很明确:动物组织匀浆成分复杂、GPx/Prx等干扰酶共存、样本量通常较大(6-10只/组 × 4-6组),比色法在特异性和通量上的双重优势在这一场景中体现得最为充分。
如果你在做植物逆境胁迫实验,检测叶片、根系等组织的CAT活性,同样推荐比色法。植物组织提取液中多酚、色素等复杂成分对紫外法的干扰几乎是灾难性的,而540 nm比色可以有效规避。此外,植物样本中也含有抗坏血酸过氧化物酶(APX)等H₂O₂清除酶,紫外法无法将其与CAT区分开来。
如果你在做纯化CAT蛋白的酶学表征——例如你从微生物中克隆表达了一种新的CAT,需要测定其Km、kcat等动力学参数——紫外法可能是更直接的选择。纯化蛋白体系中不存在其他干扰酶,背景也很干净,紫外法的连续动力学数据在这一场景下发挥出真正的优势。
如果你在做细胞实验(如细胞裂解液或培养上清中的CAT活性检测),由于细胞裂解液蛋白浓度相对较低、体积有限,比色法在样本用量和灵敏度上的优势更为突出。同时,很多培养基成分(如酚红)在紫外区有吸收,也增加了紫外法的背景干扰风险。
最后还有一个容易被忽视的场景:如果你的实验需要在同一篇论文中同时报告CAT活性和H₂O₂含量。采用紫外法时需要注意一个逻辑问题——你用H₂O₂消耗速率来反推CAT活性,又单独测定了组织中的H₂O₂含量,这两组数据在方法论上存在一定的"循环"关系。而比色法检测CAT活性的读出端是甲醛而非H₂O₂,与H₂O₂含量检测在方法论上完全独立,数据之间的关联分析更加干净。
两种方法的对比概览
为了方便快速参考,以下从几个关键维度对两种方法做一个直接的对比。
在检测原理上,紫外法追踪的是CAT催化功能介导的H₂O₂分解,比色法追踪的是CAT过氧化物酶功能介导的甲醇氧化产甲醛。在对CAT的特异性上,紫外法中等偏低(GPx、Prx等可贡献假阳性信号),比色法高(甲醇作为氢供体的反应高度特异于CAT)。在检测波长上,紫外法为240 nm(紫外区,受蛋白/核酸/酚类干扰),比色法为540 nm(可见光区,背景干净)。在检测模式上,紫外法为连续动力学法,比色法为终点法。在通量上,紫外法为逐个样本检测,比色法适配96孔板高通量。在样本用量上,紫外法需50-200 µL/反应,比色法仅需20 µL/反应。在器材要求上,紫外法需要紫外分光光度计和石英比色皿,比色法只需常规酶标仪和96孔板。在最适应用场景上,紫外法适合纯酶动力学表征,比色法适合组织匀浆、细胞裂解液等复杂生物样本的活性比较分析。
CheKine™ 微量法CAT活性检测试剂盒(KTB1040)
我们的CheKine™ 过氧化氢酶(CAT)活性检测试剂盒(微量法,货号:KTB1040)正是基于上述过氧化物酶功能原理设计的。试剂盒提供96孔板检测形式,配套预制的甲醛标准品、Purpald显色试剂和CAT阳性对照,开盒即用。
在适用样本方面,该试剂盒已在小鼠和大鼠肝脏、肾脏、脑组织匀浆,多种培养细胞裂解液,血清/血浆,以及拟南芥、水稻、小麦等植物组织提取液中验证通过。每孔仅需20 µL样本,一块96孔板可完成约40个样本的双复孔检测(含标准曲线和对照)。整个操作流程从加样到读板约60 min,适合需要批量检测的实验室。
如果你的课题还涉及SOD活性(KTB1030)、H₂O₂含量(KTB1041)、MDA含量等其他氧化应激指标,同一份样本匀浆上清液经不同倍数稀释后可以同时用于多项检测,帮助你用最少的样本构建完整的氧化损伤评价面板。
如需了解详细的操作方案或获取技术支持,欢迎联系我们。

