FAS脂肪酸合成酶活性检测试剂盒怎么选?做过几次之后才明白这些事
脂肪酸合成酶(FAS)的检测需求这几年增长很快。原因不难理解——肿瘤代谢重编程、糖尿病相关的脂质紊乱、神经炎症里的脂滴蓄积,FAS几乎都绕不开。但凡课题里涉及脂代谢表型,FAS活性就是一个绕不开的检测点。
市面上卖FAS活性检测试剂盒的厂家不少,价格相差不大,组分看起来也差不多。但真正用过几轮之后,差距就出来了——有人第一次做就出了漂亮的数据,有人反复折腾了三次还是ΔA值读不出来,最后发现问题早在选产品那一步就埋下了。
这篇文章不打算列参数表,也不想做成说明书翻译。就是把选FAS试剂盒这件事,从头到尾说清楚。
先搞清楚自己要检测的是什么
这句话听起来像废话,但很多人在这一步就模糊了。
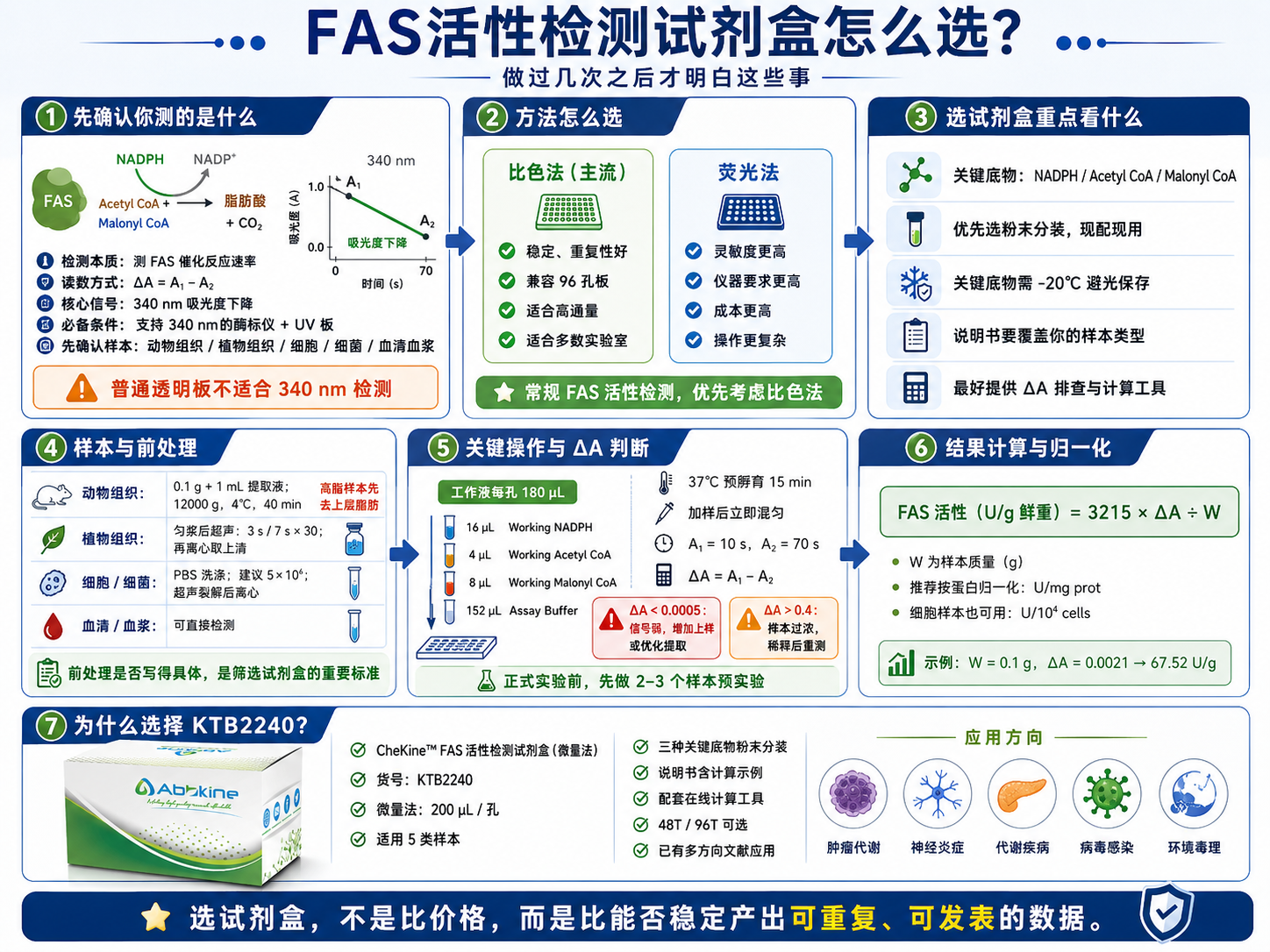
FAS活性检测,测的是酶促反应速率——具体来说,是FAS催化乙酰CoA、丙二酰CoA和NADPH合成长链脂肪酸的过程中,NADPH被消耗的速度。NADPH在340 nm有特征吸收峰,NADP⁺没有。所以只要连续测340 nm处的吸光度,看它下降有多快,就能换算出FAS活性。
这个原理决定了一件事:你选的试剂盒,最终是要上酶标仪跑的,而且必须是能测340 nm的酶标仪,用的板子必须是UV板。普通透明板在这个波段的透过率根本不达标,数据会有严重的系统误差——这不是"影响一点点",而是从根本上让结果失去意义。这一点后面还会详细说,但在选产品之前,先确认自己手头有没有合适的仪器和耗材,是最基本的前提。
另外还要想清楚,你的样本是什么类型。动物组织、植物组织、体外培养的细胞、细菌,还是血清血浆?不同样本的前处理方式差异很大,不是所有试剂盒都覆盖了全部样本类型,说明书里如果只验证了动物组织,你拿来测细菌提取物,心里就要打个问号。
检测方法这件事,比你想的更重要
目前FAS活性检测主流是两类方法:比色法和荧光法。
荧光法灵敏度更高,理论上能检测到更低浓度的样本,但对仪器的要求也更苛刻,操作过程中的环境光干扰控制更麻烦,试剂成本也更高。大多数普通实验室并不需要走这条路。
比色法,也就是基于NADPH在340 nm吸收的方法,稳定、可重复、兼容性强,配合96孔板可以同时跑大量样本,是绝大多数FAS检测需求的合理选择。微量法版本把每孔的检测体积压缩到了200 µL,样本用量少,成本可控,尤其适合那些样本量有限、需要同时检测多个指标的实验设计。
亚科因生物的KTB2240(CheKine™脂肪酸合成酶活性检测试剂盒,微量法)走的就是这条路线。原理是FAS催化底物消耗NADPH,通过测定340 nm吸光度在60秒时间窗内的下降量(A₁和A₂之差,即ΔA)来计算酶活,单次反应体系只需要200 µL,适合高通量场景。
试剂组分的细节,决定了你的数据能不能用
NADPH、乙酰CoA(Acetyl CoA)、丙二酰CoA(Malonyl CoA)——这三个是FAS活性检测的关键底物,也是最容易出问题的地方。
这三种物质都对光和温度敏感。液体形式的产品开封之后活性下降很快,如果分装工艺不好,同一批次里前几个用的和后几个用的,活性差异可能就会在数据上体现出来。粉末分装的产品在稳定性上有明显优势,使用前临时溶解,每次都是新鲜配制的工作液,批内一致性更有保障。KTB2240的三种底物均为粉末分装,使用前加入Assay Buffer溶解,现配现用,这个设计对结果稳定性是有实质帮助的。
保存条件的分级也值得关注。不是所有组分都需要-20℃,Assay Buffer在4℃就够了,但NADPH、Acetyl CoA、Malonyl CoA都需要-20℃避光保存,而且用不完的工作液要分装冻存,不能反复冻融,能在-20℃下再放两周,但超过这个时间就该扔掉了。说明书如果对这些细节语焉不详,往往意味着厂家自己也没有充分验证过长期保存的稳定性。
提取液(Extraction Buffer)同样有讲究。48T规格提供60 mL,96T提供120 mL。使用前需要提前一天从-20℃移到4℃解冻,用前再平衡到室温。这个步骤很多人嫌麻烦会跳过,结果发现提取效率不稳定,后来才知道是提取液没有充分复溶均匀。
样本类型这块,说明书里的细节很说明问题
选一款试剂盒,翻说明书的时候,看它覆盖了几种样本类型,每种类型给出的操作参数有多具体,是一个很有效的筛选维度。
KTB2240支持动物组织、植物组织、细胞、细菌和血清血浆五类样本,说明书对每一类都给出了明确的操作参数。
动物组织:取约0.1 g,加1 mL Extraction Buffer,冰浴匀浆,12000 g、4℃离心40 min,取上清。需要特别注意的是,对于脂肪含量较高的组织,比如肝脏、脂肪组织,离心后上层会有一层白色脂肪,必须小心移除,不能混入上清,否则后续检测会受到严重干扰。这个细节很多说明书不提,但做过的人都知道,少了这一步数据会非常难看。
植物组织的处理比动物组织多一步超声,功率20%或200 W,超声3 s、间隔7 s、重复30次,之后同样12000 g离心40 min。
细胞或细菌样本需要先用预冷PBS清洗,800 g离心2 min去掉培养液,再加Extraction Buffer超声裂解,参数和植物组织一样,之后12000 g、4℃离心40 min取上清。收集的细胞量建议在5×10⁶左右,太少了酶活信号会很弱。
血清血浆最简单,直接加样检测,不需要额外前处理。
工作液的配制,是一个容易被低估的环节
很多人第一次做FAS检测,按照说明书把底物都溶好了,然后直接开始加样。后来数据出来ΔA值小得可怜,反复排查,最后发现是工作液没有在37℃预孵育。
说明书上写得很清楚:配好的工作液,要在37℃孵育15 min以上,再开始检测。这一步是让底物充分活化,酶促反应才能在加入样本后快速启动。跳过这步,反应启动延迟,60秒的检测窗内捕捉到的ΔA值就会偏低,严重时几乎读不到变化。
工作液的配制比例也要严格执行:每孔180 µL工作液,其中包含16 µL Working NADPH、4 µL Working Acetyl CoA、8 µL Working Malonyl CoA,以及152 µL Assay Buffer。比例不对,底物浓度偏低,同样会压低ΔA值。
工作液要现配现用,配好之后避光冰上放置,不用了不能直接放回冰箱,要分装在避光管里,-20℃保存,两周内用完,禁止反复冻融。这些细节不是可选项,是保证批内稳定性的基本要求。
关于UV板,这件事真的绕不开
用普通透明酶标板做340 nm检测,是一个很常见的错误,而且很多人一直没发现,因为数据"看起来也有变化"。
问题在于,普通聚苯乙烯板在340 nm波段的透过率很低,不同孔之间的背景吸光度可能相差很大,这个误差叠加在NADPH消耗引起的ΔA上,会让你的结果变得完全不可靠。有时候看起来ΔA挺正常,但实际上背景噪音占了大头,真实的酶活信号被掩盖了。
UV板(紫外透明板)在340 nm处的透光率是专门优化过的,是做这类检测的标配。如果实验室里一时找不到UV板,用普通板子临时顶一下的想法,最好还是打消掉。数据出来之后如果出了问题,你可能根本找不到真正的原因在哪里。
酶标仪在开始检测前要预热30 min以上,调好波长,这是基本操作,但在赶时间的时候经常被省掉,这是个小细节,但省掉之后会让早期孔和晚期孔的数据系统性地不一致。
数据读取和ΔA值的解读
加入工作液之后,要立即混匀,然后开始计时。记录第10 s时的吸光度作为A₁,第70 s时的吸光度作为A₂,两者之差就是ΔA。
ΔA值的合理范围很重要。如果ΔA小于0.0005,说明信号太弱,可以适当增加上样量,或者检查样本提取是否充分。如果ΔA大于0.4,说明样本浓度过高,超出了线性范围,需要用Extraction Buffer稀释样本之后重新检测。
一个值得关注的细节是:这款试剂盒在包装上每个规格额外提供10%的量,用于预实验。正式开始全量检测之前,建议先选2-3个预期差异较大的样本做一轮预实验,摸清楚自己这批样本的大致ΔA范围,再决定最终的上样量和稀释倍数。跳过预实验直接大批量跑的,出了问题就是整批重做。
结果计算这件事,比看起来复杂
FAS活性的计算公式涉及NADPH摩尔消光系数(6.22×10³ L/mol/cm)、96孔UV板的光径(0.5 cm)、反应体系总体积、样本质量或细胞数量等多个参数,不同的归一化方式(按质量、按细胞数、按液体体积、按蛋白浓度)对应不同的单位,换算起来很容易出错。
KTB2240的说明书里给出了四种计算方式的完整推导过程,并且直接给出了简化公式。以最常用的按样本质量计算为例:
FAS酶活(U/g鲜重)= 3215 × ΔA ÷ W
其中W是样本质量(g)。这个简化公式已经把所有常数折进去了,直接套用就行。
说明书里还附了一个计算示例:0.1 g小鼠脾脏,测得ΔA = 0.0021,代入公式得FAS活性 = 3215 × 0.0021 ÷ 0.1 = 67.52 U/g。有了这个例子,整个计算逻辑就很清楚了。
另外亚科因生物在官网技术中心提供了在线计算工具,输入ΔA和样本参数,自动输出活性值,减少手动计算出错的可能。在同时跑几十个样本的时候,这个工具能省不少时间。
结果的归一化,是被低估的重要步骤
很多人拿到FAS活性数据之后,直接就开始比组间差异,但如果不同组的样本取样量、细胞密度或者蛋白含量本来就有差异,这个比较是不公平的。
标准做法是对蛋白浓度进行归一化,把FAS活性换算成每mg蛋白的酶活单位(U/mg prot),消除样本间的个体差异和取样误差。蛋白定量推荐用BCA法,亚科因生物自己有配套产品(KTD3001),方法成熟、操作简便,和KTB2240配合使用是比较常见的搭配。
对于细胞样本,还可以按细胞数量归一化,单位是U/10⁴细胞,这在比较不同处理组的细胞样本时尤其常用。
从文献角度来看这款产品
一个检测试剂盒有没有被同行认可,发表文献是最直接的证明。
KTB2240已经出现在多篇发表于重要期刊的研究中,覆盖的研究方向相当多样:淋巴瘤领域,有发表于Leukemia的研究探讨ZDHHC21/FASN轴作为弥漫大B细胞淋巴瘤治疗靶点;神经科学方向,有研究关注FAS乙酰化对创伤性脑损伤后小胶质细胞脂滴蓄积和炎症反应的调控;代谢疾病方向,有研究聚焦于CPT1A乙酰化与糖尿病肾病中肾小管线粒体功能障碍的关系;病毒感染领域,有PLoS Pathogens上的研究探讨FAS对HSV-1感染动态的影响;此外还有环境毒理方向的研究,关注PET微塑料对猪胰腺脂毒性的诱导机制。
这些文献横跨肿瘤、神经、代谢、感染和环境毒理五个方向,这对于审稿人来说是有说服力的背书——当你在方法部分引用这款试剂盒时,不是在使用一个没有文献记录的产品,而是一个已经在同行评审文章中经过验证的检测工具。
写在最后,选产品这件事的底层逻辑
选FAS活性检测试剂盒,本质上是在选一套能给出可重复、可发表数据的实验体系。
便宜一点的产品,如果说明书语焉不详、样本类型覆盖不全、关键组分稳定性存疑,省下来的钱可能远不够补偿你在预实验、返工、数据核对上浪费的时间。更不用说数据出了问题,在组会上被导师或同门当场指出来,那种尴尬是没有办法用价格弥补的。
具体到操作层面,选之前可以对照几个问题:说明书是否给出了你手头样本类型的详细前处理参数?关键底物是粉末分装还是液体?有没有明确说ΔA异常时怎么排查和调整?有没有配套的在线计算工具?有没有已发表文献可以引用?
KTB2240(CheKine™脂肪酸合成酶活性检测试剂盒,微量法)在这几个维度上都给出了清晰的答案。适合动物组织、植物组织、细胞、细菌和血清血浆五类样本,三种关键底物均为粉末分装,说明书提供了完整的计算公式和实际数据示例,配套在线计算器,有多篇高质量文献引用记录,48T和96T两种规格可以根据样本量灵活选择。
如果你的课题涉及脂代谢表型分析,FAS活性是一个需要认真对待的检测点。在这个点上把工具选对,后续的实验会省去很多不必要的麻烦。

