盐胁迫和干旱处理后,植物脯氨酸含量(PRO)怎么检测?
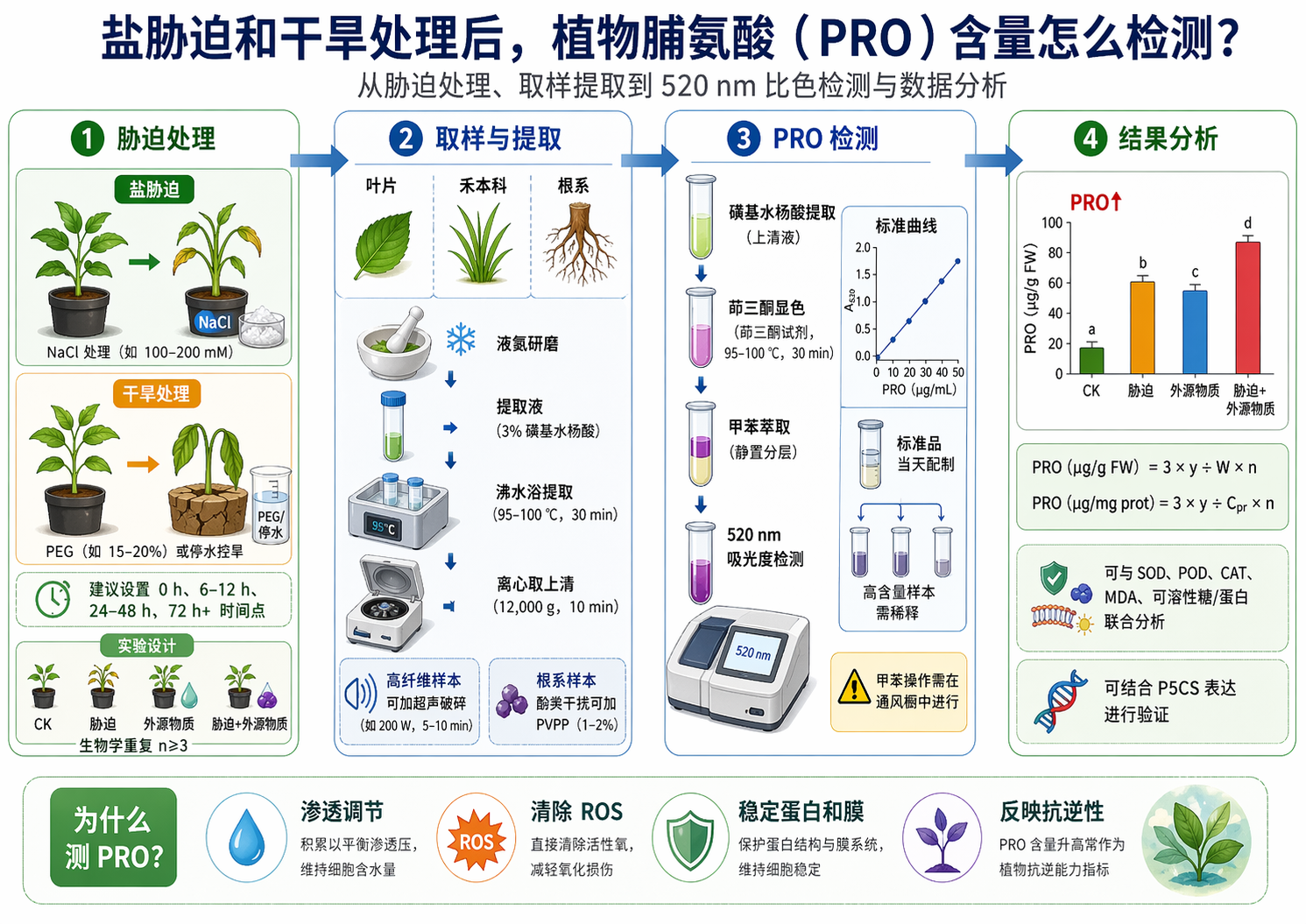
做植物逆境的人都知道脯氨酸(PRO)要测,但为什么要测、什么时候测、怎么测才准,这三个问题能同时答清楚的并不多。这篇文章从原理到操作完整走一遍,包括一些实验设计层面的考量,不只是把步骤列出来。
脯氨酸为什么是逆境研究的核心指标
植物遭受盐胁迫或干旱处理后,细胞内的渗透压会发生剧烈变化。为了对抗这种变化,植物启动渗透调节机制,在细胞内积累大量相容性溶质——脯氨酸就是其中最重要的一种。
PRO的积累不只是被动的渗透调节。它同时也是活性氧(ROS)的清除剂,能稳定蛋白质和细胞膜的结构,在胁迫解除后还可以作为碳源和氮源被快速降解利用。换句话说,PRO含量高的植物,通常意味着它在逆境下调动了更完整的防御体系。
正因如此,抗逆性强的品种往往在胁迫后积累更多的PRO,而这个积累量的差异,可以作为品种间抗逆能力比较的生理指标之一。近年来发表在 Journal of Plant Growth Regulation(2025)的燕麦耐盐机制研究——《Integrative Analysis of Physiological Properties and Transcriptome Reveals the Mechanism of Salt Tolerance in Oat (Avena sativa L.)》——就将PRO含量作为核心生理表型指标,与SOD、POD、MDA联合分析,结合转录组数据系统揭示了燕麦耐盐的分子机制。这种"多生理指标+组学"的双线策略,目前在植物逆境研究中越来越普遍。
实验设计:在做实验之前要想清楚这几件事
胁迫浓度怎么定
不同物种对盐和干旱的耐受阈值差异很大,没有一个通用浓度。盐胁迫实验里,拟南芥这类盐敏感型植物用100–150 mM NaCl通常就能产生明显效应;水稻等中等耐盐作物大概在150–200 mM;燕麦这类相对耐盐的物种可能需要到200–300 mM才能观察到显著的生理响应。
如果不确定自己的材料适合什么浓度,建议先做一轮预实验,设几个梯度处理72小时,观察表型,找"出现明显胁迫症状但植株还没死"对应的浓度区间,再以此为基础设计正式实验。
干旱处理的方式更多样——停水法、PEG模拟渗透胁迫、土壤含水量控制等,需要根据你的实验体系选择。用PEG-6000模拟干旱时,浓度通常在10%–20%之间,但有一点需要注意:PEG溶液的实际渗透势(水势)不只取决于浓度,还受环境温度影响,相同浓度在不同温度下产生的水势可能相差较大。如果你的实验对水势有精确要求,或者需要跨实验室、跨文献进行比较,建议参考Michel & Kaufmann(1973)的经典公式核算实际水势,或者直接引用目标物种已发表文献中使用的处理参数,而不是只按百分比配制。浓度同样建议预实验确认。
取样时间点的安排
这一点被很多人忽视,但它直接决定你能观察到什么。
植物在逆境下PRO的积累不是线性的。通常是胁迫开始后逐渐升高,在某个时间点达到峰值,之后可能维持高位,也可能随着胁迫时长增加或植株适应而有所回落。如果只设一个取样时间点,你采到的可能是峰值,也可能是回落阶段,得出的结论完全不同。
建议至少设置4–5个时间点,覆盖早期响应(处理后6–12小时)、中期积累(24–48小时)和后期适应或损伤(72小时以上)。0小时的未处理对照是必须保留的,它是所有后续数据的基线。
另外,如果实验跨越了光暗交替节点,不同时间点采到的数据可能混杂了昼夜节律的影响。最简单的做法是:所有时间点的取样固定在同一个光照阶段内。
对照组怎么设
最基础的设计是一个处理组加一个空白对照(CK)。如果你的实验还涉及外源物质对逆境的缓解效应(比如褪黑素、硅、纳米硒等),建议扩展为2×2的析因设计:CK、单独胁迫、单独外源物质、胁迫+外源物质四组。这样才能区分外源物质的效应究竟是直接影响了PRO代谢,还是通过缓解胁迫损伤间接改变了PRO积累。
生物学重复至少3个(n≥3),统计分析必须基于生物学重复而非技术重复——这是审稿人必查的点,不要搞混。
样本制备
不同类型的植物材料,前处理方式不一样。
叶片组织(双子叶植物为主)
称取约0.1 g新鲜叶片,加1 mL Extraction Buffer,液氮研磨后冰浴匀浆,沸水浴振荡提取10分钟,10000 g常温离心10分钟,取上清冷却待用。
这类样本通常没有太大的前处理难度,但有两个细节容易出问题:一是称样精度,0.1 g这个数字后面结果计算要用到,偏差太大会直接影响最终数值;二是沸水浴时EP管盖一定要盖紧,30分钟的加热过程中水分蒸发会导致体系浓缩,吸光度偏高。
禾本科植物(小麦、燕麦、水稻等)
这类样本的情况复杂一些。禾本科植物茎叶富含纤维素和木质素,单纯匀浆往往破碎不充分,PRO释放不完全,检测值会系统性偏低。
解决方案是在匀浆之后增加超声破碎:功率200 W,超声3秒、间隔7秒,重复30次,全程冰浴。超声头要插到液面以下,别刚好接触液面,那样效率很差。超声结束后再放沸水浴提取,步骤和叶片样本一致。
用这类样本做实验之前,建议先确认你的试剂盒说明书里有没有针对高纤维组织的前处理说明。有些产品只写了常规植物组织的方案,没有超声步骤的参数,操作起来要靠自己摸索。
根系样本
根系含有大量酚类化合物,容易对颜色反应产生干扰。提取上清颜色偏深、空白管吸光度偏高,通常是根系样本的常见问题。这种情况可以尝试加入少量PVPP(聚乙烯吡咯烷酮)吸附酚类物质后再离心。
检测步骤
标准品配制、体系配制、沸水浴、甲苯萃取这四个步骤的完整操作流程可以参考《脯氨酸含量测定实验全流程方案:样本处理、显色反应到结果计算一次说清》,这里不重复,只说几个在植物逆境样本里容易出问题的地方。
标准品要当天配。 稀释后的标准液不稳定,4小时内必须用完。很多人图省事提前一天配好放冰箱,第二天用,标准曲线的线性就已经有问题了。
盐胁迫处理组样本PRO含量往往很高。 正式检测之前最好用1–2个样本先跑一遍,看ΔA值落在什么区间。如果ΔA已经接近1.5,说明浓度超出检测上限,需要用Extraction Buffer稀释后再测,计算时记得乘稀释倍数。
甲苯萃取这步必须在通风橱里进行。 甲苯挥发性强,对神经系统和造血系统有毒性,加样、振荡、吸取上层这整个过程都不能在开放台面操作。手套、口罩、实验服是基本防护,不能省。萃取后要耐心等分层,两相分层不清楚就吸,容易把下层水相带进去,数据会偏低而且不稳定。脂质含量高的样本分层较慢,必要时可以低速离心(500 g,1分钟)辅助一下。
结果计算与数据表达
测完吸光度之后,算ΔA,代入标准曲线方程得到浓度值y(µg/mL),再根据你的实验需求换算:
按样本鲜重(最常用):
PRO(µg/g FW)= 3 × y ÷ W × n
按蛋白浓度(盐胁迫导致组织脱水时更准确):
PRO(µg/mg prot)= 3 × y ÷ Cpr × n
W是样本鲜重(g),Cpr是蛋白浓度(mg/mL),n是稀释倍数。
这里有一个值得注意的选择:高盐处理后植物叶片可能脱水萎蔫,同样质量的鲜组织里实际细胞数量和蛋白含量可能与对照组不同。如果你的实验里处理组和对照组的叶片外观差异明显,建议同时测总蛋白含量,用按蛋白浓度归一化的结果作为主要数据,按鲜重的结果作为辅助数据,在文章里都呈现出来并说明你的选择理由。
和其他指标放在一起分析
PRO含量单独看能说明的问题有限。植物逆境研究里更有说服力的是把它放进完整的生理指标体系里。
典型的搭配是PRO、可溶性糖、可溶性蛋白三个渗透调节指标联合,再加上SOD、POD、CAT酶活性和MDA含量构成的氧化损伤评估体系。一个完整的抗逆性强的品种,在胁迫下通常表现为PRO和可溶性糖显著积累、抗氧化酶活性上调、MDA含量维持在较低水平。反过来,如果PRO积累量高但MDA也同步升高,说明渗透调节没能完全抵消氧化损伤,植株的耐受是有代价的。
如果你的课题还包含转录组数据,PRO含量的变化可以与脯氨酸合成限速酶P5CS的基因表达水平进行关联验证。转录水平上调但酶活和PRO含量没有相应变化,或者反过来,都是值得深入分析的异常信号,往往能挖到更有意思的调控机制。
写文章的时候怎么呈现这部分数据
Methods里描述PRO检测方法,通常需要包含:检测原理(磺基水杨酸提取,茚三酮比色,520 nm)、使用的试剂盒名称和货号、活性单位定义、归一化方式。步骤不需要逐条列出,审稿人可以通过货号查说明书,写太细反而显得不专业。
Results里PRO数据通常以柱状图呈现,不同处理组或不同品种间的比较加显著性标记。如果同时展示多个生理指标,做成组合图要比分开几个独立图显得更整洁,也更能让审稿人一眼看到各指标的协同变化。
方法参考:CheKine™ 脯氨酸(PRO)含量检测试剂盒(微量法),货号 KTB1430 | 技术咨询:400-6800-830

