生物材料研究为什么要做DPPH实验:氧化应激、纳米载体与抗氧化验证逻辑
如果你的研究方向是纳米药物、仿生载体、功能性水凝胶,DPPH这个词你可能是在别人的Materials and Methods里第一次见到的。它不像细胞毒性、载药量、释放曲线那样看起来和材料研究直接相关,却越来越频繁地出现在这个领域的高水平文章里。
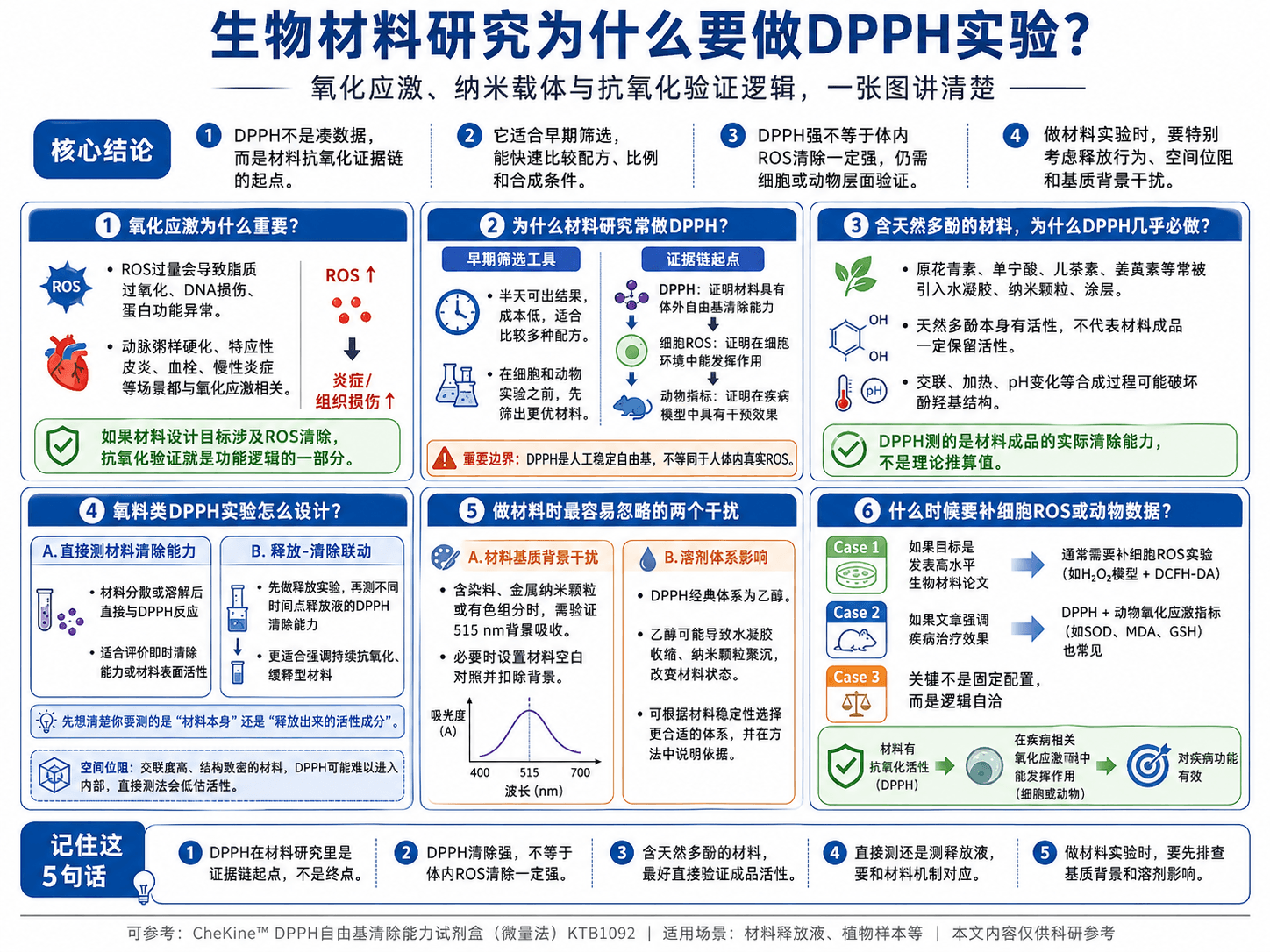
这篇文章想解释的是:这不是凑数据,而是有具体逻辑的。
从疾病机制说起:氧化应激为什么这么重要
动脉粥样硬化、特应性皮炎、血栓、慢性炎症——这些看上去机制各异的疾病,有一个共同的病理基础反复出现在文献里:氧化应激(Oxidative Stress)。
氧化应激的本质是活性氧(ROS)的产生速率超过了机体的清除能力,导致细胞膜脂质过氧化、DNA损伤、蛋白质功能异常,最终推动炎症和组织损伤的恶化。在动脉粥样硬化里,巨噬细胞泡沫化和斑块形成都与ROS密切相关;在皮肤炎症里,氧化应激是角质细胞损伤和屏障功能破坏的重要驱动因素;在血栓微环境里,ROS水平同样显著升高。
这个背景决定了一件事:如果你的材料被设计用于这些疾病场景,而它恰好含有天然多酚、抗氧化小分子、或者本身具有ROS清除能力的结构单元,那"这个材料能不能清除自由基、清除能力有多强"就不是一个可有可无的问题,而是材料功能逻辑的核心一环。
材料的抗氧化能力,凭什么要用DPPH来证明?
这是很多做材料的研究生心里的真实疑问。
直觉上,DPPH是个化学实验,测的是试管里的反应,和材料在体内的行为隔着十万八千里。为什么不直接做细胞ROS实验,或者动物模型的氧化应激指标,绕过这个体外方法?
原因有两个层次。
第一,体外化学方法是最快的筛选工具。 材料开发阶段往往需要比较大量配方、比例、合成条件的差异。细胞实验和动物实验成本高、周期长,不适合用来做早期筛选。DPPH法半天出结果、成本极低,在你还不确定哪个配方最优的时候,它是最高效的初步筛选手段。
第二,体外数据和体内数据是互补关系,不是替代关系。 高水平期刊的审稿逻辑通常是这样的:DPPH数据证明材料中的活性成分本身具有自由基清除的化学能力;细胞水平的ROS实验证明这个能力在细胞环境里可以真实发挥;动物模型证明它在体内的疾病干预效果。三个层次的数据彼此支撑,缺掉任何一层都会被问"你怎么知道材料真的在清除ROS"。
DPPH数据是这个证据链的起点,不是终点。
但这里有一个必须说清楚的科学事实:DPPH是人工合成的氮中心稳定自由基,在自然界和人体内根本不存在。 人体氧化应激产生的是氧中心自由基——超氧阴离子、羟基自由基、过氧化氢等。一个材料对DPPH清除能力强,不能直接画等号说明它对生理ROS的清除能力也强,两者的化学反应机制有根本差异。
这正是高水平审稿人越来越要求在DPPH之外补充其他数据的原因——比如ABTS(覆盖更广的自由基类型)、或者直接测H₂O₂清除能力。把DPPH的边界想清楚,文章结论才不会写过头。
含天然多酚的材料:DPPH几乎是必做的实验
原花青素、单宁酸、儿茶素、姜黄素——这些天然多酚化合物近年来在生物材料领域非常活跃,被大量引入水凝胶、纳米颗粒、涂层体系,原因之一正是它们天然具有的抗氧化活性。
但"天然多酚本身有抗氧化活性"和"你合成的含多酚材料保留了这个活性"是两件不同的事。材料的合成过程(交联、加热、pH变化)可能部分破坏多酚的酚羟基结构,从而降低实际的抗氧化能力。DPPH实验直接测的就是材料成品的清除能力,而不是理论推算值。
从这个角度说,如果你做的是含天然多酚的功能材料,不做DPPH实验,审稿人完全有理由问你:"你怎么知道合成过程没有破坏活性?"这个问题没有好的回答方式,除了补数据。
做材料研究,DPPH实验的设计和植物提取物有什么不同?
最核心的区别是你在测什么。
植物提取物直接溶于提取液检测,测的是提取物整体的清除能力,没有歧义。
含多酚的复合材料,通常有两种测法,分别回答不同的问题:
测材料的直接清除能力: 将材料分散或溶解于合适的溶剂,直接加入DPPH工作液反应。这个结果反映的是材料在接触自由基时的即时清除能力,适合评价材料表面或者快速释放部分的抗氧化活性。
测材料的释放-清除联动: 先做释放实验,取不同时间点的释放液进行DPPH检测。这个结果反映的是材料随药物缓释过程中持续提供抗氧化能力的特性,更符合材料在体内长时间工作的实际场景,对于缓释型材料来说这个数据更有说服力。
两种设计选哪个,取决于你的材料机制和文章的核心论点。如果你强调的是"持续抗氧化",释放-清除联动的数据更相关;如果你强调的是"材料本身的抗氧化性能",直接测更直接。
不过这里有一个材料类实验特有的问题需要提前想到:空间位阻效应。 小分子多酚(比如植物提取物)溶于溶液,可以和DPPH充分接触反应。但如果是交联程度高的水凝胶或者致密的纳米颗粒,材料内部的活性位点被基质包裹着,DPPH分子可能根本渗透不进去,测出来的清除能力会系统性偏低——而且你没办法知道低估了多少。
遇到这种情况,释放液测法通常比直接测材料更能反映真实的抗氧化潜力,因为释放出来的小分子可以和DPPH充分接触。如果你的材料结构致密、交联度高,在设计实验时最好把这个问题提前考虑进去,而不是等数据出来发现偏低才开始想原因。
一个容易踩的坑:材料基质的背景干扰
做植物提取物的时候,颜色干扰主要来自深色样本自身在515 nm的吸收。做生物材料的时候,还有另一个潜在的干扰来源:材料基质本身。
大多数水凝胶基质(透明质酸、明胶、聚乙二醇)在515 nm没有显著吸收,影响不大。但如果你的材料里含有染料(荧光标记)、金属纳米颗粒、或者本身有颜色的组分,必须先验证基质在515 nm是否有背景吸收,必要时设置材料空白对照,从测定值里扣除背景,否则数据不可信。
还有一个容易被忽略的问题:DPPH经典实验在乙醇体系中进行,但生物材料的实际工作环境是生理水相。 乙醇可能导致水凝胶收缩变形、纳米颗粒聚沉,改变材料的原本形态,从而影响测定结果的代表性。如果你的材料对有机溶剂敏感,可以考虑使用含少量乙醇的缓冲液体系作为折中方案,或者在方法描述里注明溶剂体系的选择依据,让审稿人知道你考虑过这个问题。
这一步很多做材料的人没想到,等数据出来发现清除率异常偏高,才开始回头排查,浪费时间。
细胞ROS实验是必须配套的吗?
取决于你的文章定位。
如果是发生物材料领域的高水平期刊(Biomaterials、ACS Nano、Advanced Materials等方向),单独的DPPH数据通常不够,细胞水平的ROS验证基本上是审稿人的预期。常用的是H₂O₂诱导氧化应激模型配合DCFH-DA荧光探针,操作不复杂,但需要提前建立细胞氧化应激模型。
如果是作为疾病治疗效果的配套数据,DPPH体外验证+动物模型的氧化应激指标(SOD、MDA、GSH等)组合也很常见,细胞实验反而不是必须的。
没有一个固定的标准配置,关键是数据之间的逻辑自洽:材料有抗氧化活性(DPPH),这个活性在疾病相关的氧化应激环境里能发挥作用(细胞或动物水平),所以材料对疾病有治疗效果(功能实验)。这条线讲得通,数据就够用。
写在最后
DPPH实验进入生物材料领域,不是凑数据的结果,是氧化应激作为疾病机制被越来越重视的必然延伸。如果你的材料在设计逻辑上涉及ROS清除,这个数据早晚要做,不如在实验设计阶段就想清楚它在你的证据链里扮演什么角色。
如果你需要一款能兼容不同类型样本(包括材料释放液)、操作规范清晰的DPPH检测工具,可以了解一下 CheKine™ DPPH自由基清除能力试剂盒(微量法)KTB1092。

