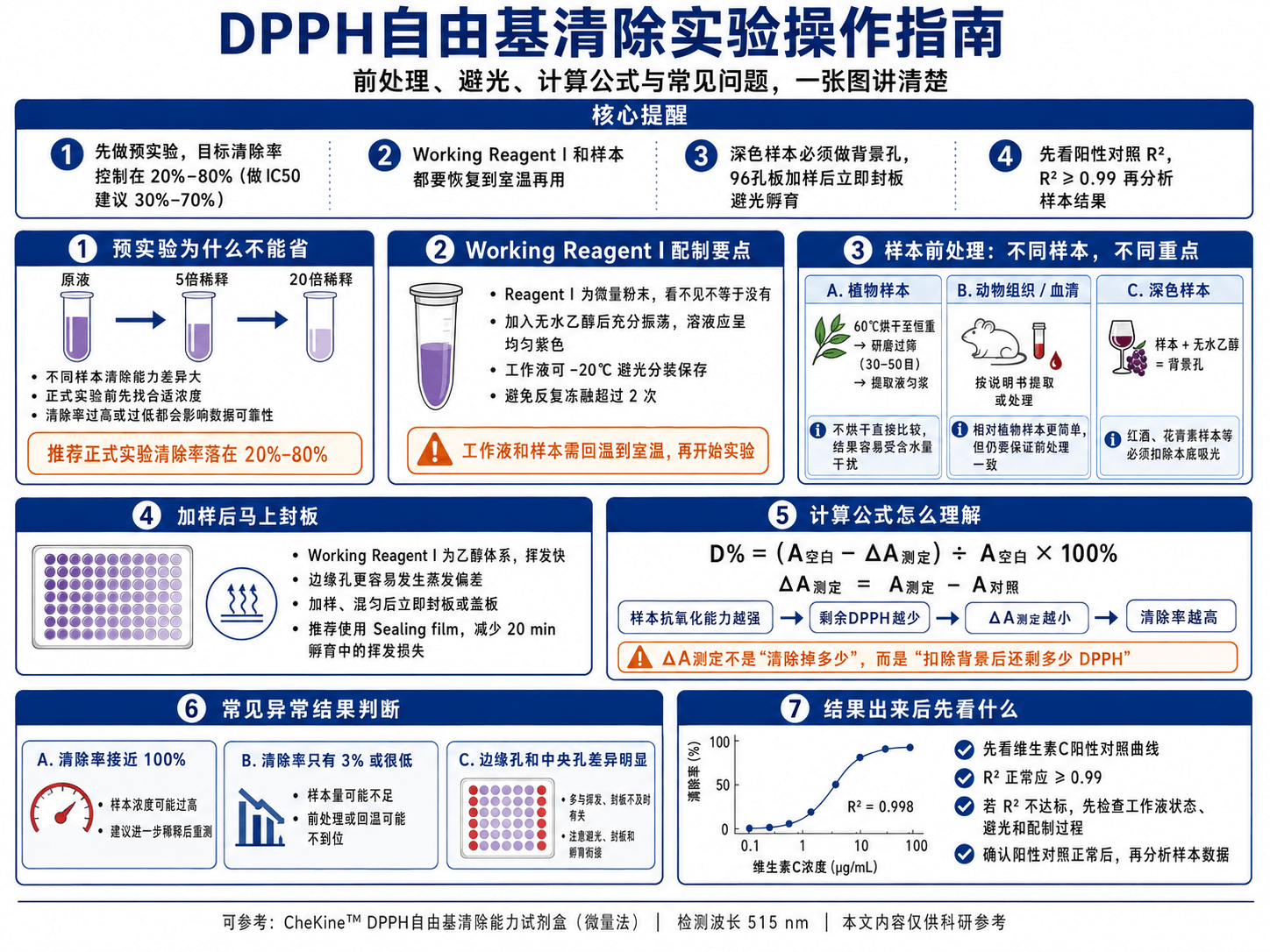
DPPH自由基清除实验操作指南:前处理、避光、计算公式与常见问题
第一次做DPPH实验的时候,我照着说明书把每一步都走了一遍,结果出来,一半样本清除率接近100%,另一半只有3%。我以为是试剂盒坏了,折腾了将近一周,最后发现是自己对这个实验的理解有根本性的偏差。
后来带新同学做实验,发现大家踩的坑几乎都一样。所以这篇文章不讲步骤,说明书里都有——我想聊的是那些说明书默认你已经知道、但你其实不知道的事。
预实验不是"谨慎的人才做的事"
很多人把预实验理解成锦上添花,觉得操作规范了就可以直接跑正式实验。DPPH实验里,这个想法会让你付出整批数据作废的代价。
原因很简单:不同样本的DPPH清除能力可能相差十几倍。植物提取物浓度稍高一点,清除率就奔着90%去了;血清稀释不够,可能根本检测不到信号。说明书给的加样量(10 µL样本)只是一个起点,不是适合所有样本的通用参数。
预实验的目的只有一个:找到合适的样本浓度。目标是让清除率落在**20%-80%**之间——这个范围内线性关系稳定,数据最可靠。如果你的实验需要进一步计算IC₅₀值,要求更严,30%-70%是更稳妥的控制范围,两端的线性在分析化学上是公认的偏差区。做法很简单,选2-3个样本,同时跑原液、稀释5倍、稀释20倍三个浓度,半天出结果,能省掉后面好几天的麻烦。
Working Reagent I看不见,但它真的在那个管子里
第一次配试剂的人几乎都有同一个恐慌:Reagent I是粉末,量极少,对着光看管底什么都看不到,很难相信里面真的有东西。
它确实在里面。用无水乙醇直接加进管里溶解,充分振荡,溶解后是紫色的,这时候你就知道它在了。配好的工作液颜色越均匀越好,如果颜色偏淡或者有细小颗粒,再振荡一会儿。
用不完的工作液-20℃避光分装保存,但有一条铁律:不能反复冻融超过两次。每次分装的量最好是一次实验的用量,用多少取多少,剩下的不要反复拿进拿出。
还有一件事很多人不在意:工作液和样本都要恢复到室温再用。 刚从冰箱取出的工作液直接加样,孔内温度偏低,反应速率慢,20分钟孵育结束时还没到平衡,读出来的清除率会系统性偏低——而且你很难知道是这个原因,因为每个孔都低,不像随机误差那么好发现。
植物样本:烘干这步不能省,也不能糊弄
做植物样本的时候,我见过最常见的省略操作是:新鲜叶片直接匀浆,不烘干。
这不是省时间,是让结果失去意义。
新鲜植物材料的含水量差异极大,同一种植物不同叶龄、不同生长状态下,含水量可能差两三倍。你称的是0.05 g样本,但里面实际的干物质量差了多少,没人知道。后面跑出来的清除率,比的是含水量,不是抗氧化活性,数据没有任何可比性。
60℃烘箱烘到恒重——"恒重"的判断是间隔两小时称量两次,差值小于0.5 mg。不是烘几个小时就算,是要真的稳定下来。烘完研磨过筛,再称样、匀浆、离心。这个前处理比动物组织麻烦得多,但没有捷径。
深色样本不是麻烦,是需要多加一个步骤
红酒、花青素含量高的浆果提取物、深色植物提取液——这些样本在515 nm本身就有吸收。你测到的吸光度下降,有一部分是DPPH被清除导致的,还有一部分是样本自己的颜色压低了数值。两者叠加在一起,清除率会虚高。
解决方案不是换样本,是多设一种孔:样本背景孔(样本加无水乙醇,不加Working Reagent I),单独读一个背景吸光度,从测定值里扣掉。操作上多十分钟,但没有这一步,深色样本的数据基本上没法用。
第一次做红酒样本时跳过这步、清除率高得离谱,大概是做DPPH实验最常见的错误之一。
加完样,马上盖板
这件事说明书里提到了避光孵育,但有一个细节没说清楚:96孔板里的Working Reagent I是乙醇体系,挥发速度比水溶液快得多,边缘孔尤其明显。
加完样之后如果在操作台上多放几分钟再盖板,边缘孔的浓度已经悄悄变化了。不同孔的蒸发量不同,数据就会出现边缘孔系统性偏离中央孔的现象——这种误差很难通过重复实验消除,因为每次都会发生。
还有一个更细的问题:96孔板自带的普通硬盖缝隙较大,对醇类挥发的阻隔效果有限,20分钟孵育期间仍然会有持续蒸发。更严谨的做法是换用专用封板膜(Sealing film),贴合更紧密,能有效控制孵育过程中的挥发损失,边缘孔和中央孔的数据一致性也会明显更好。
加样结束、混匀,封板或盖板,立即送进孵育箱,中间不要停。
计算公式有一个地方很反直觉
清除率公式是:D% = (A空白 - ΔA测定) ÷ A空白 × 100%
其中ΔA测定 = A测定 - A对照。
反直觉的地方在这里:ΔA测定越小,清除率越高。
很多人第一次看到这个公式,直觉上觉得"ΔA测定代表被清除的量",所以越大越好——但实际上ΔA测定代表的是扣除样本背景后,孔里还剩多少DPPH,不是清除了多少。样本抗氧化能力越强,DPPH被清除得越多,剩余的越少,ΔA测定越小,A空白 - ΔA测定越大,清除率才越高。
搞错这个逻辑,就会算出负的清除率,然后开始怀疑自己哪步操作出了问题——其实只是公式理解反了。
结果出来之后,先看阳性对照
拿到数据第一件事,不是看样本,是看阳性对照曲线的R²。
维生素C的标准曲线R²正常应该≥0.99。如果低于这个值,说明这次实验的Working Reagent I状态有问题,可能配制时溶解不完全、放置时间太长、或者经历了不该有的光照。这种情况下样本的数据也不可信,需要重跑。
先确认阳性对照没问题,再看样本数据,是每次实验结束后应该养成的习惯。
最后说一句
DPPH实验本身不复杂,但它对操作细节的容忍度比很多比色法实验都低——避光、温度、醇体系挥发、深色样本背景,每一个细节都能在结果上留下痕迹。第一次跑的时候多花点时间把这些逻辑搞清楚,后面每次实验都会顺很多。
如果你用的是 CheKine™ DPPH自由基清除能力试剂盒(微量法),说明书里对各类样本都有独立的前处理方案,异常结果也有对应的处理建议,碰到问题可以直接对照查。

