为什么加了样本之后溶液会从紫色变黄?——DPPH自由基检测原理,从化学到操作逻辑
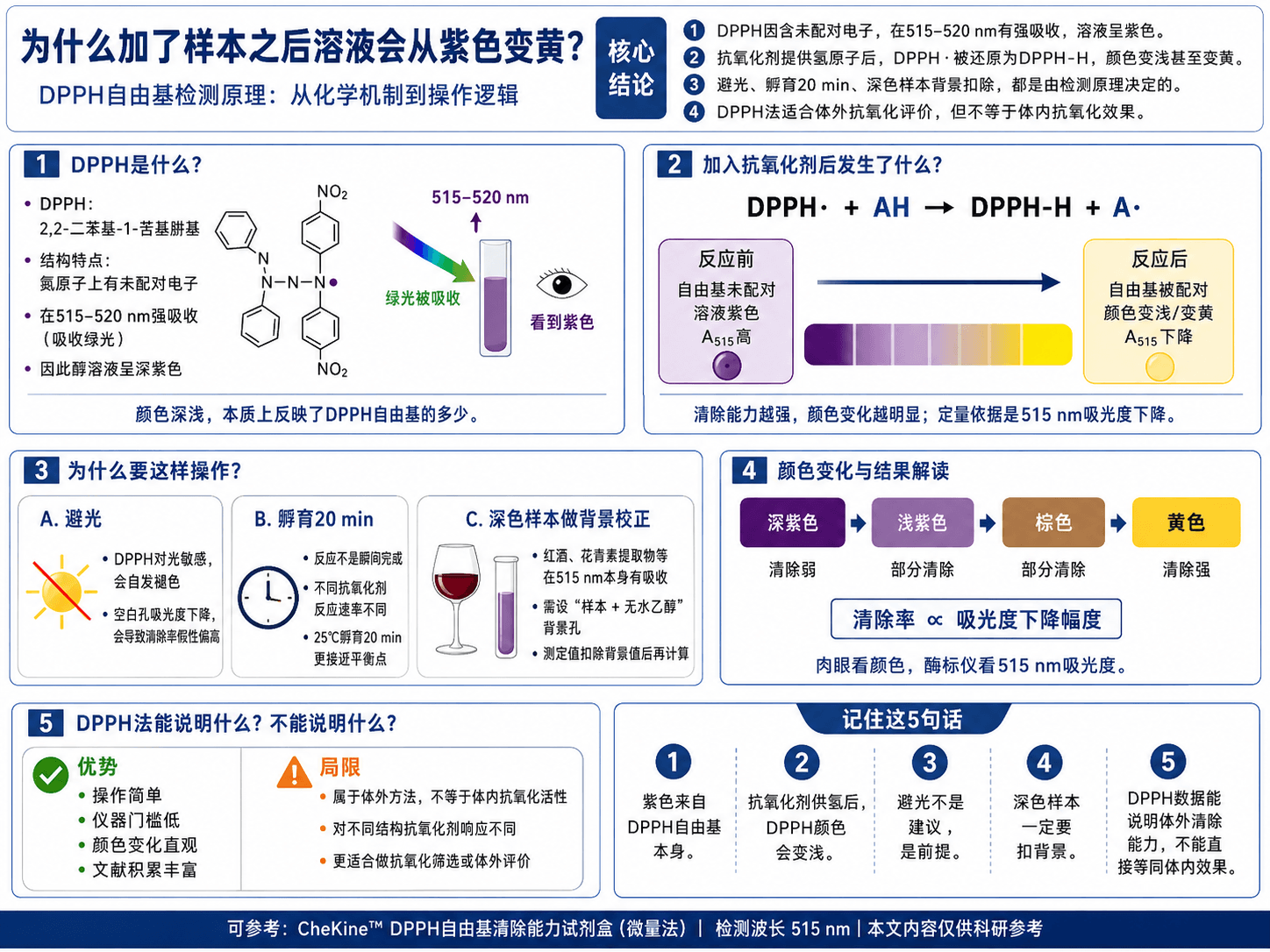
很多人做了好几轮DPPH实验,说得清步骤,但说不清楚为什么要这么做。避光是为什么?为什么要等20分钟再读数?深色样本为什么会出问题?这些问题的答案都藏在原理里。这篇文章从化学机制出发,把"知其然"和"知其所以然"串在一起。
一、DPPH是什么?为什么它是紫色的?
DPPH的全称是2,2-二苯基-1-苦基肼基(2,2-diphenyl-1-picrylhydrazyl),这串名字记不住没关系,重要的是它的结构特征:氮原子上有一个未配对的自由电子。
这个孤单的自由电子,正是DPPH一切行为的根源。
在有机化学里,含有未配对电子的分子在可见光范围内往往有强烈的吸收。DPPH的吸收峰在515-520 nm,这个波长对应的是绿光,绿光被吸收了,透过去的是紫光,所以DPPH的醇溶液看上去是深紫色。这不是染料或者颜料,是自由基本身的颜色,是那个孤立电子贡献的。
浓度越高,颜色越深,在515 nm处的吸光度值越大——这就是整个检测的物理基础。
二、加入抗氧化剂之后发生了什么?
抗氧化剂(AH)遇到DPPH自由基(DPPH·),会发生一个氢原子转移反应:
DPPH· + AH → DPPH-H + A·
DPPH自由基接受了氢原子之后,那个孤立的自由电子被配对了,分子结构发生变化,515 nm处的强烈吸收随之消失——完全反应后溶液会从紫色变成黄色。但实际实验中DPPH很少被100%清除,更常见的现象是紫色变浅、或者整体转为棕色。看到棕色不代表实验出了问题,它只是说明DPPH被部分清除,剩余的DPPH和生成的DPPH-H混在一起,呈现出介于紫色和黄色之间的过渡色。
颜色变化越明显,说明抗氧化剂提供氢原子的能力越强,清除自由基的能力也越强。用酶标仪量化这个颜色变化(测515 nm吸光度下降了多少),就能得到一个可比较的清除率数值。
整个反应逻辑非常干净:有没有清除能力,颜色说了算;清除了多少,吸光度说了算。
三、这个原理直接决定了操作上的几个"为什么"
为什么要全程避光?
DPPH自由基对光照非常敏感。可见光能量足以激发DPPH分子,导致自由基的自发分解——不需要任何抗氧化剂,仅仅是光照,DPPH就会缓慢褪色。
这意味着如果你的空白孔(只有DPPH工作液,不含样本)在光照下放了一会儿,它的吸光度已经不是初始值了。用一个已经下降的空白值去计算清除率,结果必然偏高。实验室里有时候会出现"空白样本也有清除率"的离谱数据,大多数情况下都是这个原因。
从配制工作液开始到读数结束,避光不是建议,是保证数据有效的前提。
为什么要等20分钟再读数?
DPPH自由基和抗氧化剂的反应不是瞬间完成的。不同结构的抗氧化物质,反应速率差异很大——有些多酚类化合物的氢转移反应需要数分钟才能达到平衡。
如果加样后立刻读数,你测到的是反应进行到一半的结果,不是终点值。不同样本反应速率不同,提前读数会把"反应快慢"的差异引入到本来应该只反映"清除能力强弱"的数据里,让结果之间的可比性下降。
25℃孵育20分钟是大量文献验证过的反应平衡时间点,不同样本在这个时间点基本都能到达稳定状态。
为什么深色样本会出问题?
回到原理:检测依赖的是515 nm处吸光度的变化。如果样本本身在515 nm有吸收(比如花青素、原花青素含量高的提取物,或者红酒),那么测定孔里的吸光度就同时包含了两部分:DPPH剩余量贡献的吸光度,加上样本颜色贡献的吸光度。
你以为吸光度下降是因为DPPH被清除了,但实际上有一部分下降是样本颜色在515 nm的本底吸收把数值压低的结果。
解决方案是设置样本背景空白孔:用相同体积的样本加无水乙醇(不加DPPH工作液),单独读一个背景吸光度,然后从测定值里扣除这部分背景。这一步对颜色浅的样本影响不大,但对深色样本来说,不做这一步的数据基本上不可信。
四、为什么DPPH法能成为经典方法?
DPPH法从上世纪50年代就开始被使用,历经几十年仍然是体外抗氧化评价的主流手段之一,原因很简单:
操作门槛低,不需要特殊设备,普通酶标仪或分光光度计就够;结果直观,颜色变化肉眼可见;文献积累量大,数据之间横向可比。
近年来从植物化学、食品科学延伸到生物材料领域——水凝胶、纳米颗粒、仿生载体的抗氧化性能验证,研究者也开始把DPPH法引入,原因也是同样的:操作简单,结果说得清,审稿人看得懂。
五、DPPH法做不到什么?
既然要讲原理,就不能只讲优点。
它是体外方法,不等于体内抗氧化活性。 DPPH自由基是氮中心自由基,溶解在乙醇体系里,跟生物体内真实的氧化应激环境差距很大。体外清除率高的样本,到了体内不一定有同等效果,中间还隔着吸收、代谢、分布等一系列生理过程。把DPPH清除率直接等同于"对人体的抗氧化效果"是常见的误读。
它对不同结构的抗氧化剂有偏好。 提供氢原子速率快的化合物(比如维生素C、某些黄酮类)在DPPH法里表现突出;一些通过其他机制发挥抗氧化作用的物质(比如螯合金属离子的化合物)在DPPH法里可能被低估。这也是为什么完整的抗氧化评价体系通常不只用一种方法。
了解这两个局限,不是为了否定DPPH法,而是知道自己的数据能说明什么问题、不能说明什么问题,结论才写得准确。
写在最后
DPPH原理本身不复杂,但理解了氢转移反应、自由基配对、515 nm吸收这些底层逻辑之后,避光要求、孵育时间、深色样本的背景校正——这些操作细节就不再是需要死记的规定,而是自然而然的推论。实验出了问题,你也更容易找到根源,而不是靠排列组合去试。
如果你正好在搭建抗氧化检测体系,或者需要一款操作流程和异常处理都说明清楚的试剂盒,可以了解一下 CheKine™ DPPH自由基清除能力试剂盒(微量法)——从样本前处理到结果计算,各类样本类型都有独立的操作方案。

