肿瘤免疫研究中为什么要检测NO一氧化氮?从γδT细胞代谢研究说起
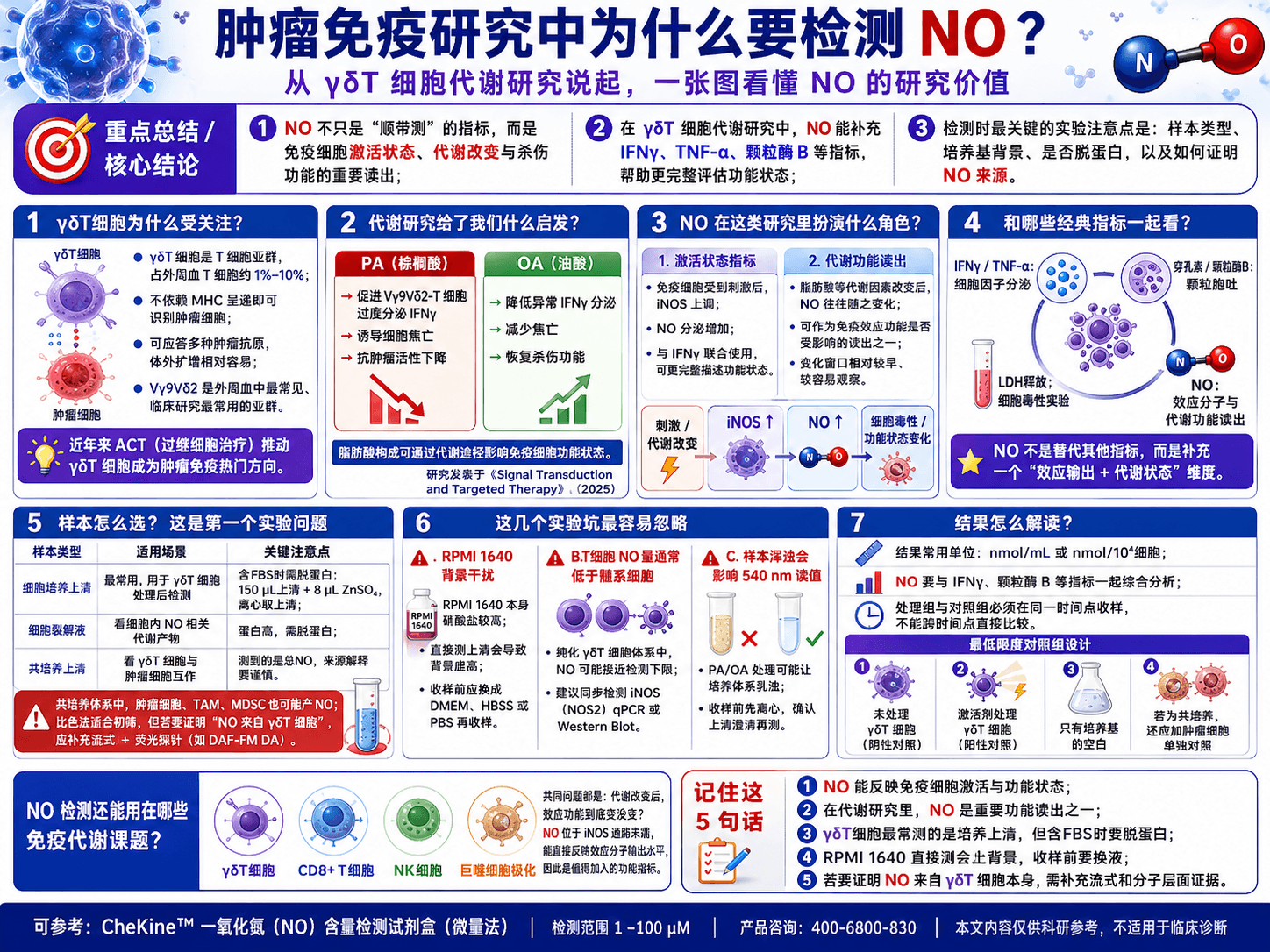
做肿瘤免疫的同学,提到检测指标,第一反应通常是细胞因子——IFNγ、TNF-α、IL-2这些。NO经常被忽略,或者被当成一个顺带测的边角指标。
但如果你的课题涉及免疫细胞的代谢状态、激活程度,或者细胞毒性功能评估,NO其实是一个很有价值的指标,而且很多时候是其他指标替代不了的。
γδT细胞是什么,为什么最近这么热
γδT细胞是T细胞里的一个亚群,占外周血T细胞的1%–10%,长期以来没有αβT细胞受关注。但近几年情况变了。
原因是过继细胞治疗(ACT)领域的进展。γδT细胞有几个特点让它在肿瘤治疗里很有吸引力:不需要MHC呈递就能识别肿瘤细胞,可以对多种肿瘤抗原产生应答,而且体外扩增相对容易。Vγ9Vδ2亚群是外周血里比例最高的γδT细胞,也是目前临床研究里用得最多的。
发表于《Signal Transduction and Targeted Therapy》(2025)的研究,就是围绕这个亚群展开的。研究发现,接受γδT细胞治疗的癌症患者,血清里棕榈酸(PA)和油酸(OA)的水平与治疗效果有关联。进一步的机制研究揭示了一个此前不太清楚的路径:PA会刺激Vγ9Vδ2-T细胞过度分泌IFNγ,诱导细胞焦亡,最终导致抗肿瘤活性下降;而OA能逆转这个过程,降低IFNγ分泌、减少焦亡、恢复杀伤功能。
这个发现的意义不只是"油酸对γδT细胞有好处",而是说明饮食脂肪酸的构成会通过代谢途径影响免疫细胞的功能状态,这给γδT细胞治疗的临床前研究提出了一个新的变量。
NO在这类研究里扮演什么角色
γδT细胞的抗肿瘤功能,核心是"杀伤能力"。评估这个能力,通常会从几个维度来测:细胞因子分泌(IFNγ、TNF-α)、颗粒胞吐(穿孔素、颗粒酶B)、细胞毒性实验(LDH释放)……NO就在这个框架里。
NO由诱导型一氧化氮合酶(iNOS)催化合成,是免疫细胞激活之后的效应分子之一。活化的巨噬细胞、NK细胞和部分T细胞亚群,在受到刺激后会释放NO,直接对肿瘤细胞产生细胞毒性。
在γδT细胞的研究里,NO有两个层面的意义:
一是作为细胞激活状态的指标。γδT细胞受到肿瘤抗原或细胞因子刺激后,iNOS表达上调,NO分泌增加。测NO可以反映细胞被激活的程度,和IFNγ一起用,能更完整地描述细胞的功能状态。
二是在代谢研究里作为功能读出。像PA/OA这类脂肪酸影响细胞代谢的研究,NO是判断代谢改变有没有影响免疫效应功能的一个指标之一。细胞代谢状态变了,NO分泌量往往也会跟着变,这种变化早于很多下游表型,检测窗口相对宽。
做这类实验,样本选择是第一个问题
γδT细胞相关的NO检测,样本来源主要是这几类:
细胞培养上清:体外扩增的Vγ9Vδ2-T细胞,经过PA或OA处理、或者肿瘤细胞共培养之后,收取培养上清检测NO。这是最常用的方式,操作也不复杂。不过如果培养体系里含有FBS,这类上清蛋白含量高,需要先脱蛋白再检测——150 µL上清加8 µL ZnSO₄,离心取上清,这一步不能省。
这里有一个绕不过去的问题:培养基的选择。RPMI 1640是淋巴细胞和免疫细胞培养最常用的培养基,但它本身含有较高浓度的硝酸盐,直接拿去测NO,背景值会虚高,实验组和对照组的差异全被掩盖掉。
处理方式是在收样前换掉培养基,换成DMEM、HBSS或PBS,培养一段时间再收上清检测。这一步很多人做到一半才想起来,导致前面的样本白收了。
细胞裂解液:如果需要测细胞内的NO相关代谢产物,裂解之后取上清检测。这类样本蛋白含量高,需要脱蛋白处理之后再用。
共培养体系的上清:γδT细胞和肿瘤细胞共培养,收上清来测。这种情况需要提前想清楚一个问题:测到的NO到底是谁产的。肿瘤微环境里,肿瘤细胞本身、肿瘤相关巨噬细胞(TAM)和髓系来源抑制细胞(MDSC)都是产NO的大户,共培养上清里测到的是总浓度,靠设对照组做减法在逻辑上说得通,但这套证据在投稿时不一定能说服审稿人。如果你的课题需要证明"是γδT细胞本身在特定代谢状态下产生了NO",比色法测上清是一个初筛的方式,但更严格的证据链需要流式细胞术结合荧光探针(比如DAF-FM DA)来补充——流式可以直接圈定Vγ9Vδ2细胞亚群,看单细胞层面的NO变化,溯源更直接。
另外还有一个量级的问题值得注意:iNOS高表达是活化巨噬细胞的标志,但T细胞(包括γδT细胞)产NO的绝对量通常远低于髓系细胞。如果你的体系里没有巨噬细胞、只有纯化的γδT细胞,信号有可能徘徊在检测下限附近。遇到这种情况,建议同步用qPCR检测iNOS(NOS2)基因表达,或者Western Blot跑iNOS蛋白,多个维度的证据放在一起,结论才站得住脚。
结果怎么解读
NO检测结果通常以nmol/mL或nmol/10⁴细胞来表示,跟IFNγ、颗粒酶B这些指标放在一起,构成免疫细胞功能的综合评估。
几个解读的时候要注意的地方:
处理组和对照组的时间点要一致。 NO是动态分泌的,不同时间点收的样本之间不能直接比。PA处理24小时和48小时的NO水平可能完全不一样,时间点不一致会让结论混乱。
注意PA/OA处理本身对培养基的影响。 这类脂肪酸在培养体系里有时会形成乳浊液,影响上清的澄清度,进而影响540 nm的吸光度读值。收样前先离心一次,确认上清澄清再测。
对照组的设计要完整。 最少要有:未处理的γδT细胞(阴性对照)、激活剂处理的γδT细胞(阳性对照)、只有培养基的空白。如果是共培养体系,还需要单独的肿瘤细胞对照。
这个研究方向还在往哪里走
脂肪酸代谢影响免疫细胞功能,这个方向近两年发表的工作越来越多,不只是γδT细胞。CD8⁺T细胞、NK细胞、巨噬细胞极化,都有类似的研究在做。
共同的问题是:代谢改变之后,效应功能到底变没变,变了多少? NO是其中一个答案,因为它处于iNOS通路的末端,直接反映效应分子的输出水平,不像上游的基因表达或者蛋白水平那么间接。
如果你的课题也在这个方向上,或者研究的是其他类型免疫细胞在不同代谢条件下的功能变化,NO检测是一个值得加进去的指标,不复杂,但能补充一个其他方法不容易直接反映的维度。
上述实验流程中涉及的NO定量,可以参考 CheKine™ 一氧化氮(NO)含量检测试剂盒(微量法)(货号:KTB1400),检测范围1–100 µM,含FBS的培养上清需脱蛋白处理,使用RPMI 1640培养的样本需提前换培养基,具体操作参数见产品说明书。
产品咨询:400-6800-830 | 本文内容仅供科研参考,不适用于临床诊断

