为什么检测一氧化氮要测NO₂⁻和NO₃⁻?从原理说清楚这件事
刚接触NO检测的同学,十个里面有八个会问同一个问题:
我要检测的是一氧化氮,为什么试剂盒操作下来测的是亚硝酸盐和硝酸盐?
这不是说明书写错了,也不是试剂盒偷懒。把这个逻辑搞清楚,后面做实验才不会一头雾水。
NO在样本里根本存不住
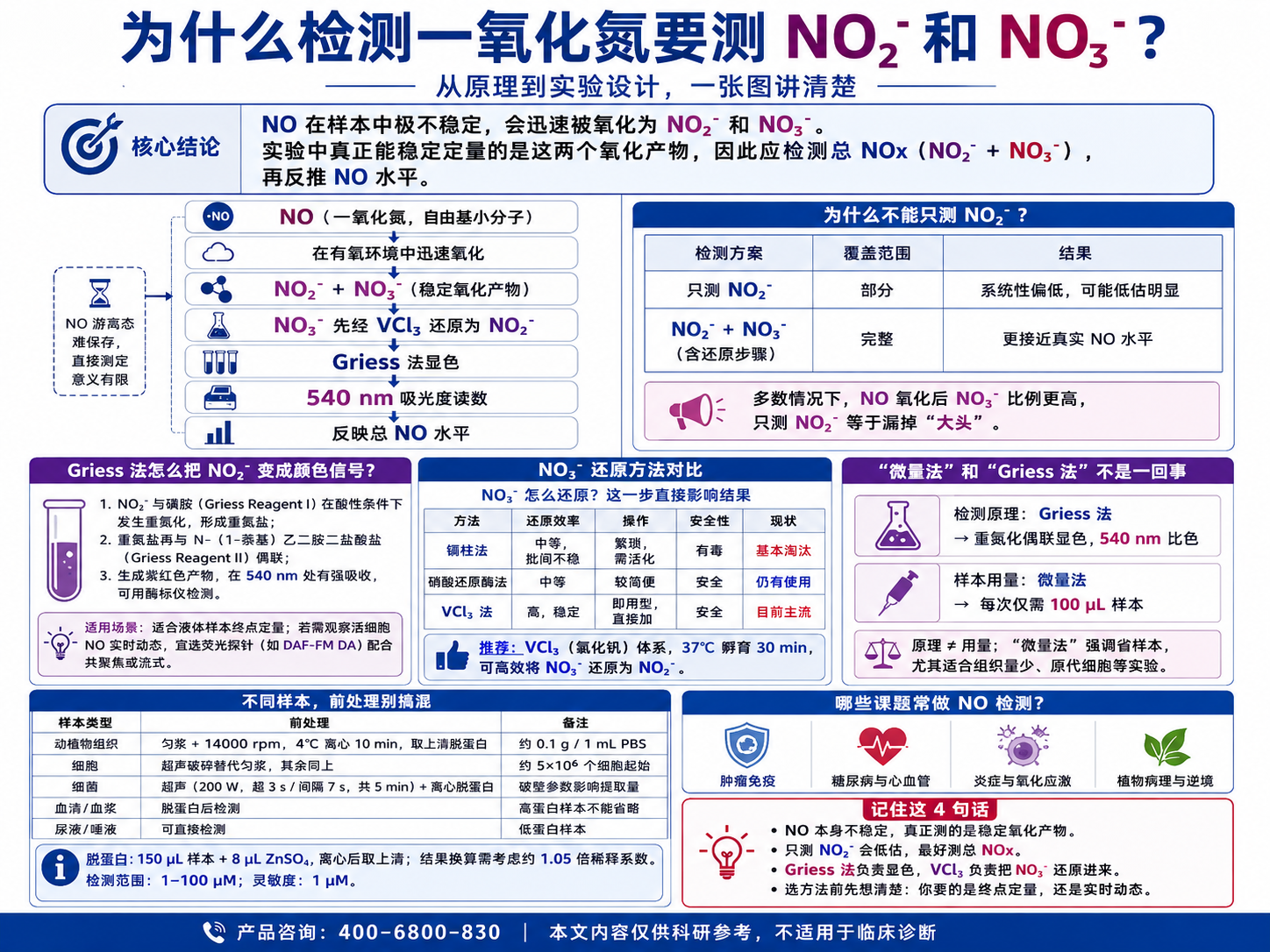
NO是个气体小分子,带自由基,在有氧环境里撑不了几秒钟就被氧化掉了,最后变成NO₂⁻和NO₃⁻。
你取完样本开始处理,离心、稀释、加试剂——这段时间已经足够让游离NO消耗殆尽。所以就算真有办法直接测NO,拿到的数也没有意义。
实验里真正能稳定存在、可以被定量的,是这两个氧化产物。测NO₂⁻和NO₃⁻的总量,再反推原来有多少NO,这才是现在通行的做法。
只测NO₂⁻,数据会少一截
NO氧化之后,产物里NO₃⁻的比例比NO₂⁻高得多。要是你用的方法只能测NO₂⁻、没有把NO₃⁻还原进来,等于丢掉了大头。
| 检测方案 | 覆盖范围 | 结果 |
|---|---|---|
| 只测NO₂⁻ | 部分 | 系统性偏低,有时偏差很大 |
| NO₂⁻ + NO₃⁻(含还原步骤) | 完整 | 接近真实NO水平 |
这种偏差不容易在实验里察觉,因为样本间做相对比较的时候趋势是对的,但绝对值低了一截。等写文章有人来对数据,量级对不上就麻烦了。
买试剂盒之前,先确认它到底测的是NO₂⁻单项,还是同时覆盖了两者。
Griess法怎么把NO₂⁻变成颜色信号
Griess法是现在检测NO₂⁻用得最多的比色方法,两步反应:
NO₂⁻先跟磺胺(Griess Reagent I)在酸性条件下发生重氮化,生成重氮盐;重氮盐再跟N-(1-萘基)乙二胺二盐酸盐(Griess Reagent II)偶联,出来一个紫红色复合物,在540 nm有很强的吸收,酶标仪直接读。
这个方法实验室门槛低,普通酶标仪就够,96孔板一次跑一批,不用额外买设备。文献里用这套方法的研究足够多,审稿人看到也不会对方法本身有什么意见。
不过有一点要说清楚:Griess法适合的是液体样本的终点定量,把样本取出来处理好之后测一个静态数值。如果你的课题需要看活细胞里NO的实时释放动态,这套就不够用了,得换荧光探针(比如DAF-FM DA)配合共聚焦或流式来做。两类需求是不同的实验设计,选方法之前先想清楚自己要的是哪种数据。
NO₃⁻怎么还原,这步选错了结果差很多
Griess法负责显色,NO₃⁻到NO₂⁻的转化是另一回事,得靠还原剂单独完成。用什么还原、效率怎么样,直接影响你最后测到的数对不对。
| 还原方法 | 还原效率 | 操作 | 安全性 | 现状 |
|---|---|---|---|---|
| 镉柱法 | 中等,批间不稳 | 繁琐,需提前活化 | 有毒 | 基本被淘汰 |
| 硝酸还原酶法 | 中等 | 较简便 | 安全 | 有在用,依赖酶活性 |
| VCl₃法 | 高,稳定 | 即用型,直接加 | 安全 | 目前主流 |
VCl₃(氯化钒)加进去,37℃孵30分钟就完成还原,不用提前处理,也没有镉柱的毒性问题。改进Griess法配的就是这个体系,三个试剂现配成工作液,拿来就用。老方法能用,但VCl₃这套确实省事,还原也更稳定。
"微量法"和"Griess法"不是一回事
产品名称里这两个词同时出现,有人觉得是在重复说同一件事。其实一个说原理,一个说用量:
| 术语 | 意思 | |
|---|---|---|
| 检测原理 | Griess法 | 重氮化偶联显色,540 nm比色 |
| 样本用量 | 微量法 | 每次只要100 µL样本 |
用量这个事,做过取样困难的实验才会在意。小鼠的一小块组织,或者培了好几天的原代细胞,能少用一点是一点。跟传统比色皿法要的几个毫升比,100 µL差距不小。
不同样本前处理差别挺大,别搞混了
| 样本类型 | 前处理 | 备注 |
|---|---|---|
| 动植物组织 | 匀浆 + 14000 rpm 4℃离心10 min,取上清脱蛋白 | 约0.1 g / 1 mL PBS |
| 细胞 | 超声破碎替代匀浆,其余同上 | 5×10⁶个细胞起始 |
| 细菌 | 超声(200 W,超3 s/间隔7 s,共5 min)+ 离心脱蛋白 | 破壁参数很影响提取量 |
| 血清/血浆 | 脱蛋白后检测 | 高蛋白样本不能跳过这步 |
| 尿液/唾液 | 直接检测 | 低蛋白,不用处理 |
脱蛋白的步骤是150 µL样本加8 µL ZnSO₄混匀,离心后取上清用。这一步会引入约1.05倍的稀释,算结果的时候要带进去,不然数据会系统性偏低。很多人在这里漏掉了这个系数。
检测范围1–100 µM,灵敏度1 µM,覆盖正常生理水平到炎症激活状态。
哪些课题在用NO检测
肿瘤免疫:γδT细胞、巨噬细胞的功能评估,NO既是效应分子也是代谢状态指标。脂质代谢与免疫功能的交叉研究里用得越来越多。
糖尿病和心血管:评估血管内皮功能的经典指标,内皮损伤程度和血管舒张机制研究里基本都会涉及。
炎症和氧化应激:活化巨噬细胞产NO是经典细胞毒性机制,这类实验里NO定量是常规操作。
植物病理和逆境:病原菌互作、逆境胁迫里有稳定需求,相对小众但很固定。
文献里实际怎么用的
发表于《Signal Transduction and Targeted Therapy》的研究探讨棕榈酸对γδT细胞抗肿瘤免疫功能的影响,其中用NO检测来评估免疫细胞功能状态。样本是细胞培养上清,用RPMI 1640培养的要注意——这个培养基本身硝酸盐含量高,会干扰结果,检测前需要换成DMEM或PBS。
发表于《Advanced Science》的研究涉及稻瘟病菌侵染过程中的亚硝基化调控,NO检测用于追踪病原菌不同侵染阶段的信号变化,样本是真菌,走的是超声破碎提取方案。
两篇方向完全不同,底层检测方法一样,只是样本前处理有区别。改进Griess法在这两类实验里都能直接用。
上面这些操作细节,包括标准品配制、工作液配比、各类样本的前处理步骤,在 CheKine™ 一氧化氮(NO)含量检测试剂盒(微量法)(货号:KTB1400)的说明书里都有完整说明。有需要的可以直接联系我们索取。
产品咨询:400-6800-830 | 本文内容仅供科研参考,不适用于临床诊断

