植物抗氧化酶系统全面解析:POD、SOD、CAT的功能差异与联合检测策略
为什么需要这篇文章
如果你在数据库中搜索近五年发表的植物逆境生理研究论文,会发现一个几乎普遍的现象:极少有论文只报告单一抗氧化酶的活性数据。绝大多数研究同时检测了SOD、POD、CAT三种酶的活性,再加上MDA含量和H₂O₂含量,构成一组"氧化应激指标组合"。在投稿审稿过程中,如果你只报告了POD一项数据,审稿人几乎一定会要求你补测SOD和CAT——这不是审稿人的个人偏好,而是因为抗氧化酶系统本身就是一个协同工作的网络,只看一个节点无法得出有生物学意义的结论。
但对于很多刚进入这个领域的研究生来说,一个核心困惑始终存在:这些指标之间到底是什么关系?为什么要同时测?测出来之后又该怎么联合解读?有些指标升高是"好事"(说明植物在积极防御),有些升高却是"坏事"(说明损伤已经发生),如果不理解背后的生物学逻辑,面对一堆升升降降的柱状图,很容易写出自相矛盾的讨论。
这篇文章的目的是帮你建立一个完整的认知框架——从活性氧(ROS)的产生讲起,到各抗氧化酶如何分工配合清除ROS,再到当清除能力不足时MDA等损伤标记物如何反映氧化损伤的程度——最后落到实际的实验设计层面,讨论联合检测时各指标的选择逻辑、取材策略和数据解读方法。
第一部分:起点——活性氧(ROS)从哪里来
植物细胞中ROS的正常来源
活性氧(Reactive Oxygen Species,ROS)并不是逆境胁迫的专利产物。在正常生理状态下,植物细胞的多个代谢过程都会持续产生ROS,这是有氧代谢不可避免的副产物。
叶绿体是植物细胞中ROS的最大来源。在光合作用的光反应阶段,光系统I(PSI)的电子传递链末端会有少量电子"逃逸",直接将O₂还原为超氧阴离子自由基(O₂⁻·),这个过程被称为Mehler反应。在光系统II(PSII)侧,当电子传递链过度还原时(如光能过剩而CO₂固定不足),也会促进O₂⁻·的生成。据估计,正常光照条件下叶绿体产生的O₂⁻·可占光合电子传递总通量的1%–2%。
线粒体是第二大ROS来源。呼吸链的复合体I和复合体III在电子传递过程中也会有少量电子泄漏,将O₂还原为O₂⁻·。过氧化物酶体(Peroxisome)则是第三个重要来源——其中的乙醇酸氧化酶在光呼吸过程中直接产生H₂O₂,脂肪酸β-氧化过程中的酰基辅酶A氧化酶也会生成H₂O₂。
此外,细胞质中的黄嘌呤氧化酶和NADPH氧化酶(质膜定位,也称为Respiratory Burst Oxidase Homolog,RBOH),以及细胞壁中的某些过氧化物酶和草酸氧化酶,都是ROS的贡献者。
主要ROS种类及其化学特性
植物细胞中与抗氧化系统相关的ROS主要有四种,它们之间存在化学转化关系。
超氧阴离子自由基(O₂⁻·)是电子传递链泄漏的直接产物。它带有一个未配对电子,化学性质活泼但寿命相对较短(微秒级),且因带负电荷不易穿过生物膜,其损伤作用主要局限在产生位点附近。
过氧化氢(H₂O₂)是O₂⁻·经歧化反应或酶促反应的产物。与O₂⁻·不同,H₂O₂不带电荷、不是自由基,化学性质相对温和,但最关键的特点是它能够自由穿越生物膜。这使得H₂O₂具有独特的双重角色:一方面它是潜在的氧化损伤因子,另一方面它还充当细胞内的信号分子——参与气孔关闭、程序性细胞死亡、系统性获得抗性(SAR)等多种信号转导途径。H₂O₂的这种信号功能意味着,植物细胞并不试图将H₂O₂完全清除至零,而是将其维持在一个对信号转导有利但不至于造成损伤的浓度窗口内。
羟基自由基(·OH)是毒性最强的ROS,几乎可以无选择性地攻击所有生物大分子。它主要由H₂O₂通过Fenton反应(需要Fe²⁺或Cu⁺催化)生成。正因为·OH的反应活性极高,它的半衰期极短(纳秒级),在产生位点就地反应,无法被酶系统有效清除——唯一的防御策略是控制其上游前体(即H₂O₂和游离金属离子)的浓度。
单线态氧(¹O₂)主要在叶绿体中由PSII的光敏色素(特别是过量激发态的叶绿素)将能量转移给基态O₂而生成。¹O₂的主要靶点是脂质双分子层中的不饱和脂肪酸,是引发膜脂过氧化的重要起始因子之一。
逆境胁迫为什么会导致ROS爆发
理解了ROS的正常来源之后,就容易理解为什么逆境胁迫会导致ROS的过量积累。核心逻辑是:几乎所有的非生物胁迫(盐胁迫、干旱、高温、低温、重金属、UV-B辐射等)和生物胁迫(病原菌侵染、虫害等),都会通过不同的机制干扰电子传递链的正常运转或激活专门的ROS产生酶,导致ROS的产生速率超过清除速率。
以盐胁迫为例,高盐导致气孔关闭→胞内CO₂浓度下降→Calvin循环减速→光合电子传递链下游受体(NADP⁺)不足→电子传递链过度还原→电子泄漏到O₂增加→O₂⁻·和H₂O₂产量上升。与此同时,Na⁺的过量积累直接损伤线粒体呼吸链的蛋白复合体,进一步增加了呼吸来源的ROS。此外,盐胁迫还会激活质膜上的RBOH(NADPH氧化酶),在胞外空间产生大量O₂⁻·作为信号触发防御响应——这本身也增加了ROS的总量。
当ROS的产生速率超过清除速率时,多余的ROS会攻击膜脂(导致脂质过氧化)、蛋白质(导致羰基化修饰和功能丧失)和核酸(导致碱基氧化和链断裂),造成细胞层面的氧化损伤。植物抗氧化酶系统的生物学意义,就是尽可能维持ROS在安全浓度范围内,延缓或防止这种损伤的发生。
第二部分:三大抗氧化酶——分工明确的清除流水线
植物的酶促抗氧化系统可以形象地理解为一条"ROS清除流水线"。这条流水线上有三个核心岗位,每个岗位负责处理一种特定形态的ROS。三大酶之间是串联关系而非并联关系——上游酶的产物恰好是下游酶的底物。这种串联关系是理解"为什么必须联合检测"的钥匙。
第一站:SOD——将O₂⁻·转化为H₂O₂
超氧化物歧化酶(Superoxide Dismutase,SOD,EC 1.15.1.1)催化的反应是:
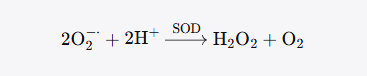
两个O₂⁻·分子在SOD催化下,一个被氧化为O₂,另一个被还原为H₂O₂。这是一个歧化反应——同一种底物既是电子供体又是电子受体。SOD的催化速率极快,接近扩散限制速率(约2 × 10⁹ M⁻¹s⁻¹),是已知最高效的酶之一。
植物细胞中存在三种类型的SOD,按照其活性中心结合的金属辅因子区分:Cu/Zn-SOD(主要分布在叶绿体基质和细胞质中)、Mn-SOD(分布在线粒体基质中)和Fe-SOD(分布在叶绿体中,某些物种的过氧化物酶体中也有)。不同亚细胞定位的SOD各自负责清除其所在区室产生的O₂⁻·。
SOD在抗氧化系统中的角色是"第一道防线"。它的重要性在于:O₂⁻·虽然本身毒性有限,但如果不被及时清除,会通过Haber-Weiss反应和Fenton反应间接生成毒性极强的·OH。SOD通过快速将O₂⁻·转化为化学性质相对温和的H₂O₂,从源头上切断了·OH的主要生成路径。
但SOD的工作只完成了清除流水线的第一步——它的产物H₂O₂仍然是一种ROS,浓度过高时依然有害。因此,SOD活性升高后,如果下游清除H₂O₂的酶跟不上,H₂O₂就会积累。这就引出了流水线的第二站和第三站。
第二站和第三站:CAT与POD——两条H₂O₂清除通路
H₂O₂的酶促清除在植物细胞中主要由两套系统并行承担:过氧化氢酶(Catalase,CAT)和过氧化物酶(Peroxidase,POD),它们在底物亲和力、催化效率、亚细胞定位和调控方式上各有特点,形成了功能互补的关系。
CAT(EC 1.11.1.6) 催化的反应极为简洁:
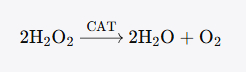
CAT直接将两分子H₂O₂分解为水和氧气,不需要额外的电子供体。CAT的催化转换数(turnover number)极高,每分子酶每秒可分解约4 × 10⁷分子H₂O₂,是所有抗氧化酶中催化效率最高的。但CAT有一个显著的局限:它对H₂O₂的Km值较高(约30–100 mM),意味着它只在H₂O₂浓度较高时才能高效工作。换句话说,CAT是一个"应急处理大户"——当H₂O₂浓度因为胁迫而急剧升高时,CAT发挥主力清除作用。
在亚细胞定位上,植物CAT主要集中在过氧化物酶体中,这与其功能高度匹配——过氧化物酶体是光呼吸和脂肪酸β-氧化过程中H₂O₂产量最大的区室,需要高效的就地清除机制。在叶绿体和细胞质中,CAT的分布很少甚至缺失,这些区室的H₂O₂清除主要依赖其他途径。
POD(EC 1.11.1.7) 催化的反应需要一个氢供体(以AH₂代表):
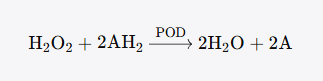
与CAT不同,POD在分解H₂O₂的同时需要氧化另一个底物分子。在植物体内,这个氢供体可以是酚类化合物、抗坏血酸(维生素C)、谷胱甘肽等多种还原性物质。POD对H₂O₂的Km值远低于CAT(通常在微摩尔级别),这意味着POD即使在H₂O₂浓度较低时也能有效工作——它是一个"精细调控者",负责在日常水平下维持H₂O₂的稳态平衡。
植物POD的亚细胞分布极为广泛:细胞壁、液泡、细胞质和叶绿体中都有分布。特别值得注意的是,植物POD家族的基因数量非常庞大——拟南芥中有73个、水稻中有138个POD编码基因——这些同工酶在不同组织、不同发育阶段和不同胁迫条件下有差异化的表达模式,赋予了植物极为精细的区室化H₂O₂清除能力。
此外,植物POD的功能不仅限于ROS清除。细胞壁定位的POD还参与木质素合成、木栓质沉积和交联反应,这些都是植物构建物理屏障抵御病原菌侵入的重要机制。因此,胁迫条件下POD活性的升高,可能同时反映了ROS清除需求的增加和物理屏障构建的加强——这种功能双重性在解读POD数据时需要考虑。
补充角色:抗坏血酸-谷胱甘肽循环(AsA-GSH循环)
除了CAT和POD之外,植物叶绿体中还有一套精密的H₂O₂清除机制——抗坏血酸-谷胱甘肽循环,也称为Asada-Halliwell循环。这个循环涉及四种酶:抗坏血酸过氧化物酶(APX)首先将H₂O₂还原为水并将抗坏血酸(AsA)氧化为单脱氢抗坏血酸(MDHA);MDHA可以自发歧化为脱氢抗坏血酸(DHA);脱氢抗坏血酸还原酶(DHAR)利用还原型谷胱甘肽(GSH)将DHA还原回AsA;氧化型谷胱甘肽(GSSG)再由谷胱甘肽还原酶(GR)利用NADPH还原回GSH。
APX对H₂O₂的Km值比CAT低一个数量级以上(微摩尔级别),是叶绿体中清除H₂O₂的主力军。在一些深入研究植物抗氧化机制的工作中,APX活性、AsA含量和GSH含量也被纳入检测指标体系,与SOD、POD、CAT一起构成更完整的抗氧化状态评估。
流水线的全景图
将以上信息整合在一起,植物抗氧化酶系统的运转逻辑可以概括为一条清晰的主线。各种环境胁迫导致电子传递链异常,O₂⁻·大量产生。SOD迅速将O₂⁻·转化为H₂O₂。H₂O₂随后由三条并行通路清除:过氧化物酶体中的CAT负责处理高浓度H₂O₂,叶绿体中的APX(通过AsA-GSH循环)处理低浓度H₂O₂,而广泛分布的POD则在多个区室中以酚类等为电子供体清除H₂O₂。如果三条通路的总清除能力仍然不足,剩余的H₂O₂在游离Fe²⁺的催化下生成·OH,·OH攻击膜脂引发脂质过氧化链式反应,其终产物之一就是丙二醛(MDA)。
这就是为什么在实验设计中,SOD、POD、CAT反映的是"防御能力",MDA反映的是"损伤程度",H₂O₂含量反映的是"防御与损伤之间的平衡状态"。
第三部分:损伤标记物——MDA与H₂O₂
MDA(丙二醛):膜脂过氧化的终产物指标
MDA是多不饱和脂肪酸在ROS(主要是·OH和¹O₂)攻击下发生脂质过氧化反应的终产物之一。严格来说,脂质过氧化的产物谱很宽,包括MDA、4-羟基壬烯醛(4-HNE)、丙烯醛等多种活性羰基化合物。MDA之所以成为最常用的脂质过氧化标记物,主要是因为它的检测方法简单——硫代巴比妥酸(TBA)比色法已有几十年的应用历史,操作简便、成本低廉。TBA法检测的是MDA与TBA在酸性加热条件下反应生成的粉红色产物(MDA-TBA₂加合物),在532 nm处有特征吸收。
MDA含量升高,说明细胞膜已经发生了氧化损伤。这一点非常重要:MDA反映的是"已经发生的损伤",而不是"正在面临的威胁"。将MDA与抗氧化酶活性放在一起解读时,逻辑应该是——如果抗氧化酶活性足以应对ROS的升高,那么MDA含量应该没有显著变化(有效防御);如果抗氧化酶活性虽然上调但仍然不足以清除所有多余的ROS,MDA就会上升(防御部分失败);如果胁迫极其严重导致抗氧化酶本身都因蛋白变性而活性下降,MDA将大幅飙升(防御系统崩溃)。
需要注意的是,TBA比色法的特异性存在争议。TBA不仅与MDA反应,也会与糖类、氨基酸和其他醛类物质交叉反应,导致所谓的"TBARS"(TBA反应物质)读数可能高估了真实的MDA水平。在精确要求高的研究中,可以考虑使用HPLC法分离MDA-TBA₂后再定量,以提高特异性。但对于大多数逆境生理研究来说,TBA比色法提供的相对比较(处理组相对于对照组的变化)已经足够用。
H₂O₂含量:防御与损伤之间的中间变量
直接测量组织中的H₂O₂含量,可以提供一个关于氧化还原状态的"实时快照"。H₂O₂含量升高,说明ROS的产生速率超过了当前清除速率(但不等于已经发生了损伤——H₂O₂需要转化为·OH才能引发膜脂过氧化)。H₂O₂含量正常,有两种可能:一种是ROS产生没有增加,另一种是ROS产生虽然增加了但抗氧化系统同步上调、维持了平衡。
常用的H₂O₂含量检测方法包括碘化钾比色法和钛盐比色法。需要注意的是,H₂O₂是一种高度不稳定的分子,取材后必须立即在液氮中速冻,提取和检测全程避免光照和金属离子接触,否则H₂O₂在样本处理过程中就会大量分解,导致结果偏低。
第四部分:联合检测的实验设计策略
指标组合的选择逻辑
并不是检测的指标越多越好。在资源有限的情况下,应该根据研究问题来选择最有信息量的指标组合。
对于一般性的植物逆境生理研究(如验证某种处理是否引发了氧化胁迫),最低限度的指标组合是"SOD + POD + CAT + MDA"四件套。SOD + POD + CAT覆盖了ROS清除流水线的两个关键节点(O₂⁻·清除和H₂O₂清除),MDA反映了清除不足时的损伤后果。这四个指标的检测方法成熟、试剂盒供应充足、文献可比性好,是审稿人最低限度的期望。
如果你的研究涉及具体的抗氧化调控机制解析(如某转录因子或基因对抗氧化系统的调控),建议在四件套基础上增加H₂O₂含量、APX活性、AsA含量和GSH含量,构建更完整的抗氧化网络评估。在部分发表于高影响因子期刊的研究中,研究者还会加入O₂⁻·的组织化学定位染色(如NBT染色)和H₂O₂的原位检测(如DAB染色),从空间维度补充酶活数据无法提供的区室化信息。
如果你的研究重点在膜损伤和细胞死亡,可以在MDA基础上增加电解质渗漏率(Electrolyte Leakage)和Evans Blue染色——前者反映膜完整性的整体变化,后者直接标记死亡细胞。
取材策略:一份组织多个指标
联合检测面临的一个实际问题是样本量需求。每个指标都需要一定量的组织来提取和检测,如果每个指标都独立取材,需要的植物材料总量可能远超实验条件允许的范围(特别是在拟南芥这种小型模式植物中)。
解决这个问题的策略是"一次提取,多重检测"。思路是将同一份组织匀浆后的上清液分别取等份用于不同指标的检测。但需要注意的是,SOD、POD和CAT的最适提取缓冲液条件可能略有差异(如pH、是否需要添加特定保护剂等),如果使用同一种提取缓冲液提取,需要确认该缓冲液不会显著影响其中任何一种酶的活性。部分厂家已经开发了兼容多种酶活检测的通用提取缓冲液,如果你计划一次提取测多个指标,选用这类兼容性经过验证的提取体系可以减少很多麻烦。
另一个实际技巧是将取来的组织在液氮中研磨成粉末后,精确称取多份粉末,分别用不同的提取缓冲液提取,用于不同的指标检测。这比分别取材要好——至少保证了所有指标的原始材料来自完全相同的组织区域和状态。
MDA和H₂O₂的提取条件与酶活指标不同(通常使用三氯乙酸而非磷酸盐缓冲液),必须独立提取,不能与酶活共用同一份上清液。
反应时间窗口的协调
在一天之内同时检测多个指标时,需要合理安排操作顺序。不同酶活检测的反应等待时间不同,如果安排不当会导致某些样本上清液在室温下等待时间过长,活性下降。
一个推荐的操作流程是:当天早上完成所有样本的匀浆和离心,获取上清液后立即置于冰上。先测反应最快的指标(通常是POD,反应时间仅1分钟),然后测SOD(如果使用NBT法,显色需要20–30分钟,可以在显色等待期间准备CAT的检测),最后测CAT(紫外法需要逐个比色皿读数,比较耗时)。MDA的提取和显色可以与酶活检测并行操作——MDA的TBA反应需要沸水浴15–20分钟,这个等待时间可以利用来读取酶活数据。
如果你使用的是同一品牌的成系列试剂盒,各试剂盒之间的操作流程和加样体系在设计上通常会有一定的兼容性(比如使用相似的缓冲液体系、相似的加样量范围),这会大大简化联合检测的操作衔接。
生物学重复数量的确定
联合检测时,每个指标都需要足够的生物学重复来支撑统计分析。一般建议每个处理组设置至少3个生物学重复(独立的植物个体),如果可能的话5–6个更好——因为抗氧化酶活性的生物学变异本身就比较大,重复数少时统计功效不足,可能检测不出真实存在的处理效应。
需要特别注意的是,如果你的实验设计包含多个时间点和多个处理浓度,总样本量会迅速膨胀。以"3个浓度 × 4个时间点 × 5个重复 × 5个指标"为例,即使每个指标可以用96孔板微量法检测(每板80个有效孔),也需要好几块板。在规划实验之前,先根据总样本量估算所需的试剂盒数量和检测工作量,避免做到一半才发现试剂不够用。
第五部分:联合数据的解读框架
典型情境一:轻度胁迫下的有效防御
在轻度或中度胁迫处理的早期阶段(如中等浓度NaCl处理24小时),研究者经常观察到的模式是:SOD、POD、CAT活性均显著上调,H₂O₂含量无显著变化或仅轻度上升,MDA含量无显著变化。
这个模式的生物学解读是:胁迫确实增加了ROS的产生速率,但植物的抗氧化系统及时响应、上调了清除能力,成功地将ROS维持在安全水平以内,未发生显著的氧化损伤。这通常被解读为植物对该胁迫条件具有较好的适应能力。
典型情境二:防御能力不足导致的氧化损伤
在高强度胁迫处理或胁迫持续较长时间后,常见的模式是:SOD和POD活性上调(可能幅度比轻度胁迫更大),但CAT活性不升反降,H₂O₂含量显著升高,MDA含量显著升高。
这个模式告诉我们:虽然SOD和POD仍在努力工作(活性上调),但H₂O₂清除系统的另一条通路(CAT)已经因胁迫导致的蛋白损伤而部分失活。H₂O₂清除能力的总体缺口导致了H₂O₂的积累,继而引发了膜脂过氧化(MDA上升)。CAT对高温和盐胁迫特别敏感——CAT的四聚体结构在高浓度NaCl或高温下容易解聚,丧失催化活性。这是在很多盐胁迫研究中CAT活性呈现"先升后降"时间曲线的分子基础。
典型情境三:抗氧化系统全面崩溃
在极端胁迫条件或胁迫后期(如超高浓度NaCl处理7天以上),可能出现:SOD、POD、CAT活性均显著低于对照水平,H₂O₂含量极高,MDA含量极高。这意味着细胞损伤已经严重到连抗氧化酶蛋白本身都大量变性降解,防御系统已经崩溃,组织正在经历不可逆的氧化损伤。在这种状态下的植物通常已经表现出明显的表型症状——叶片严重萎蔫、黄化、甚至坏死。
需要警惕的解读误区
第一个常见误区是"酶活性越高=抗性越强"的线性思维。酶活性的高低本身并不直接等同于植物抗性的高低——关键在于酶活性的上调是否足以平衡ROS的增加。一个品种在胁迫下POD活性上调了3倍,另一个品种只上调了1.5倍,不能直接得出前者抗性更强的结论——如果前者的ROS产生速率也更高,它需要更高的酶活性才能维持平衡。只有将酶活性数据与MDA、H₂O₂等损伤指标联合分析,才能判断哪个品种的防御更"有效"。
第二个误区是忽略酶活性的时间动态。抗氧化酶活性不是一个静态值,而是一个随胁迫时间持续变化的动态过程。在单一时间点取材的研究中,看到的只是这条时间曲线上的一个切面。如果两个研究取材时间不同,观察到的酶活变化方向甚至可能相反——一个在峰值前取材看到升高,另一个在峰值后取材看到下降。因此,在讨论部分比较自己的数据与他人文献时,务必注意时间点的匹配性。
第三个误区是混淆了酶活性变化的原因。POD活性的升高可能是因为POD基因表达上调(转录层面的调控),也可能是因为已有的POD蛋白被激活(翻译后修饰层面的调控),还可能是因为POD的底物可获得性增加(底物层面的调控)。在没有配套的基因表达数据(如qRT-PCR或RNA-seq)的情况下,不宜对酶活性变化做过深的机制推断。酶活性数据描述的是"功能层面的变化",机制层面的归因需要额外的实验证据。
第六部分:各指标常用检测方法概览
为了帮助初次设计联合检测方案的研究者快速了解各指标的检测方法概况,这里对主要指标的常用检测方法做一个简要介绍。
SOD活性的最常用检测方法是NBT(氮蓝四唑)光还原法。原理是:核黄素在光照下产生的O₂⁻·将NBT还原为蓝色的甲臜(Formazan),SOD通过竞争性地清除O₂⁻·来抑制甲臜的生成。反应体系中SOD活性越高,蓝色产物越少,吸光度(560 nm)越低。SOD活性以"抑制NBT还原50%所需的酶量"定义为一个活性单位(U)。这种方法灵敏度好、重现性高,是文献中最广泛采用的SOD检测法。
POD活性的最常用检测方法是愈创木酚比色法,这在本系列的另一篇文章《过氧化物酶(POD)活性检测完整实验方案:愈创木酚比色法原理、步骤与计算详解》中有详细的从原理到操作的完整讲解,此处不再重复。
CAT活性的最常用检测方法是紫外法(UV法),直接在240 nm波长处监测H₂O₂浓度的下降速率。由于H₂O₂在240 nm处有吸收,CAT催化H₂O₂分解后吸光度降低,ΔA₂₄₀/Δt即反映了CAT的催化速率。这种方法操作简单快速,但需要紫外分光光度计(酶标仪需要支持UV波段读数),且反应体系中不能含有在240 nm处有干扰吸收的物质。也有基于可见光比色法的CAT检测试剂盒(利用H₂O₂与特定显色剂的反应),适合没有紫外分光光度计的实验室。
MDA含量的检测通常采用TBA比色法,在532 nm处测定MDA-TBA₂加合物的吸光度,同时在600 nm处读取背景吸光度进行校正。
H₂O₂含量的检测可采用钛盐比色法(H₂O₂与硫酸钛在酸性条件下形成黄色过钛酸络合物,在415 nm处测定)或碘化钾比色法。
第七部分:从单一指标到系统化研究——试剂盒的选择考量
当你需要同时检测4–6个氧化应激指标时,试剂盒的选择策略与只测单一指标时有所不同。以下几点是联合检测场景下需要额外考虑的。
提取体系的兼容性是首要考量。如果你购买了不同品牌的试剂盒来分别检测不同指标,各家的提取缓冲液配方可能差异很大。这意味着你可能需要为每个指标独立提取一份样本——样本量翻了好几倍,操作时间也大幅增加。而如果你选用同一品牌的系列化产品,提取体系的兼容性通常经过了验证,有可能用一种提取液(或少数几种)覆盖多个指标的检测,大大节省样本和时间。
说明书的格式统一性也影响操作效率。在一天之内交替操作多种试剂盒时,如果每家的说明书格式和术语体系都不同,操作者需要频繁切换"上下文",增加出错概率。使用同一品牌的系列产品,说明书的术语、流程结构和计算公式格式通常保持一致,操作体验更顺滑。
经济性方面,部分厂家对系列产品的组合购买提供一定的价格优惠。在多指标联合检测的场景下,单个试剂盒的价格差异乘以指标数量后会被放大,综合性价比的比较更加重要。
以Abbkine的CheKine™系列为例,该品牌围绕植物氧化应激研究提供了一组配套的检测试剂盒,覆盖了SOD活性(货号KTB1030)、POD活性(货号KTB1150)、CAT活性(货号KTB1040)、MDA含量以及总抗氧化能力(T-AOC)等多个指标。这些产品在提取体系设计上考虑了联合使用的兼容性,说明书格式统一,且均提供多种归一化计算公式。对于计划开展系统性氧化应激评估的研究者来说,使用系列化的产品可以减少因跨品牌操作带来的额外变量,让你的精力集中在生物学问题本身而不是操作层面的适配上。
关于POD活性检测试剂盒的详细选购分析——包括样本适配性、说明书信息量、计算公式透明度等维度的逐项比较——可以参考本系列的《POD活性检测试剂盒怎么选?从样本适配到结果计算的选购避坑指南》。如果你已经进入了操作阶段并遇到了数据异常,《POD活性检测结果异常?ΔA过高/过低/波动大的原因分析与解决方案》中有针对各类常见问题的系统排查指引。
结语
植物抗氧化酶系统是一个高度协调的网络,SOD、POD和CAT各自承担清除流水线上不同节点的任务,与MDA和H₂O₂等指标共同构成了评估植物氧化应激状态的完整维度。理解这个网络中各成员的功能定位和相互关系,不仅能帮助你设计出更合理的实验方案,更能帮助你在面对一组复杂数据时讲出一个逻辑自洽的生物学故事。
无论你是刚开始接触逆境生理研究的新手,还是正在准备一轮多指标联合检测的进阶研究者,希望这篇文章提供的框架能为你的工作带来一些实质性的帮助。
相关阅读:
- 过氧化物酶POD活性检测试剂盒怎么选?从样本适配到结果计算的选购避坑指南
- 植物盐胁迫研究中过氧化物酶POD活性怎么测?实验方案、结果解读与常见问题
- 过氧化物酶(POD)活性检测完整实验方案:愈创木酚比色法原理、步骤与计算详解
- 过氧化物酶POD活性检测结果异常?ΔA过高/过低/波动大的原因分析与解决方案
本文为植物抗氧化酶系统的综述性科普文章,旨在帮助研究者理解各氧化应激指标的生物学意义和联合检测的逻辑。文中提及的CheKine™系列检测试剂盒由Abbkine出品,包括SOD活性检测试剂盒(KTB1030)、POD活性检测试剂盒(KTB1150)、CAT活性检测试剂盒(KTB1040)等,适用于动物组织、植物组织、细胞及血清等多种样本类型。产品详情及说明书下载请访问Abbkine官网。

